2024年11月15日,美国食品药品监督管理局(FDA)批准revumenib(Revuforj)用于治疗1 岁及以上成人和儿童患者赖氨酸甲基转移酶2A基因 (KMT2A) 易位的复发或难治性急性白血病患者。

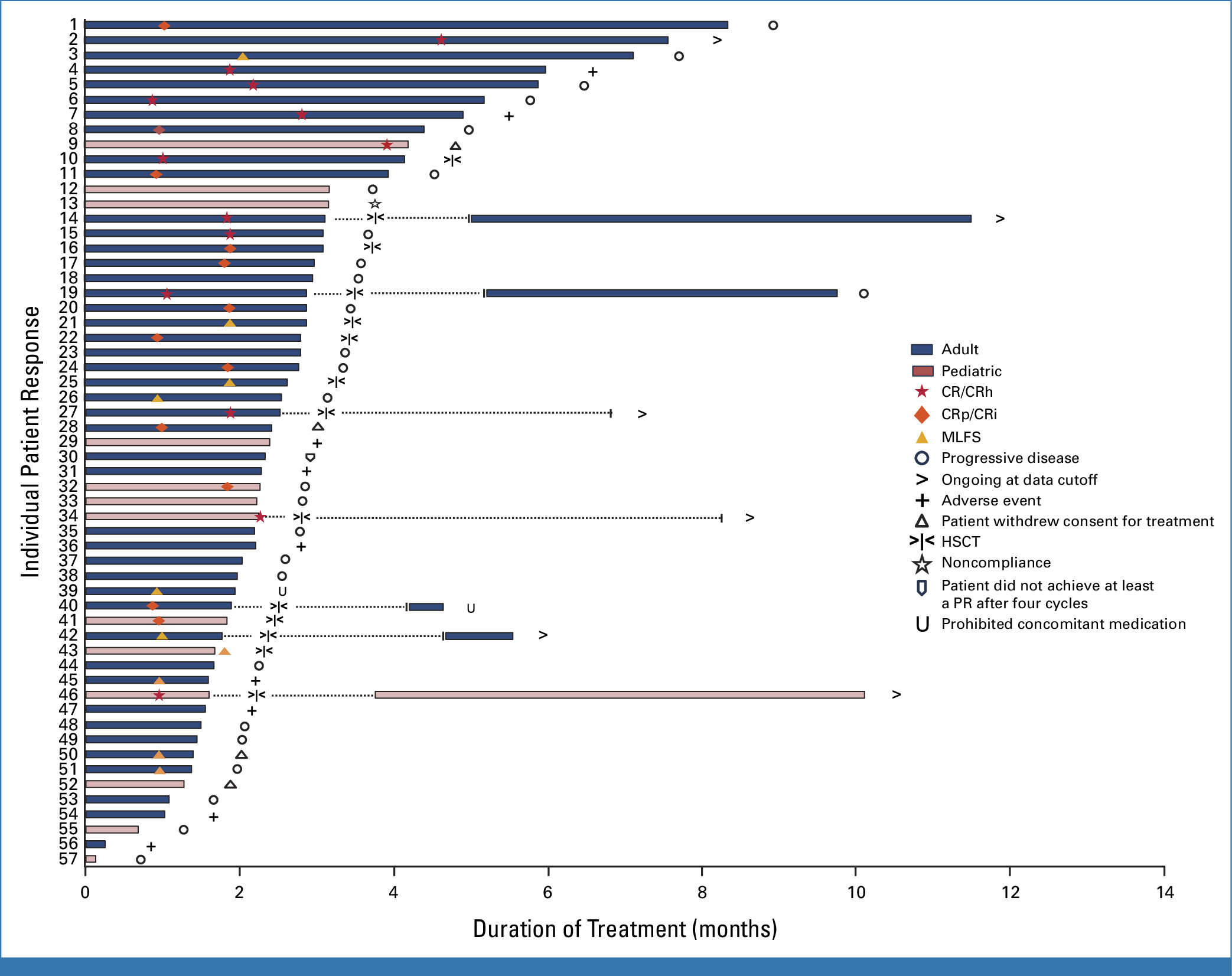
此次批准主要基于AUGMENT-101(NCT04065399)研究试验,该试验共纳入94例患者,结果显示:总缓解率(ORR)为63.2%,完全缓解(CR)率+部分血液学恢复的完全缓解(CRh)率为21.2%,中位总生存期为 8.0 个月。
最常见的不良反应 (≥20%) 是出血、恶心、磷酸盐升高、肌肉骨骼疼痛、感染、天冬氨酸氨基转移酶升高、发热性中性粒细胞减少、丙氨酸氨基转移酶升高、全段甲状旁腺激素升高、细菌感染、腹泻、分化综合征、心电图 QT 延长、磷酸盐降低、甘油三酯升高、钾降低、食欲下降、便秘、水肿、病毒感染、疲劳和碱性升高磷酸酶。
急性白血病是由造血细胞的遗传改变引起的,这些改变导致造血过程中分化受阻和细胞增殖不受控制。约10%的急性白血病患者存在KMT2A重排异常,其可见于儿童和成人几种类型的白血病中。Revumenib 是一种有效的口服小分子抑制剂,对复发或难治性KMT2A突变的急性白血病患者具有可接受的安全性。
临床试验对于传统疗法无效或疗效较差的患者来说,是寻找新的治疗药物和方法的,最快最安全的途径,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。目前有临床试验正在寻找白血病患者,患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家(400-880-3716)来寻找适合的临床研究。
参考资料
1.https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-revumenib-relapsed-or-refractory-acute-leukemia-kmt2a-translocation
2.https://ascopubs.org/doi/10.1200/JCO.24.00826?url_ver=Z39.88-2003&rfr_id=ori:rid:crossref.org&rfr_dat=cr_pub%20%200pubmed

相关推荐
随便看看
- 临床获益率达92.3%!奥雷巴替尼在TKI耐药的琥珀酸脱氢酶(SDH-)缺陷型胃肠道间质瘤(GIST)患者最新进展公布
- 索托拉西布、索托雷塞(AMG510 Lumakras)
- Dato-DXd治疗非小细细胞肺癌的II期TROPION-Lung05试验的事后分析结果公布
- 癌症肿瘤靶向治疗耐药的类型有哪几种,靶向治疗耐药的表现是什么
- 杜韦利西布,度维利塞 克必妥 Duvelisib
- 盐酸阿思尼布片获批用于新诊断的费城染色体阳性的慢性髓细胞白血病
- Carfilzomib 卡非佐米 凯洛斯 Kyprolis
- PD-1抑制剂替雷利珠单抗获批广泛期小细胞肺癌
- 安罗替尼联合派安普利单抗治疗晚期肺巨细胞癌的罕见病例
- 德曲妥珠单抗拟纳入优先审评











