热门推荐
资讯列表
2026年初,美国食品药品监督管理局(FDA)批准了iSCIB1+黑色素瘤疫苗进入Ⅲ期临床试验,数据显示该疫苗联合免疫疗法使患者16个月无进展生存率达到74%,远超当前标准方案的50%。
同月,德国BioNTech公司的mRNA癌症疫苗BNT113获得FDA快速通道资格,为HPV阳性头颈癌患者带来新希望。
...
2026年4月,西班牙研究团队宣布:针对林奇综合征(一种遗传性结直肠癌高风险疾病)患者的Nous-209疫苗早期临床试验取得突破。在45名终生患癌风险高达80%的受试者中,该疫苗引发了“强烈的免疫反应”,且未出现严重副作用。
近日,俄罗斯卫生部宣布其首款国产个性化mRNA癌症疫苗“Neooncovac”已为首位60岁的黑色素瘤患者完成了注射。这不仅是俄罗斯实验性癌症治疗计划的重要一步,更是标志着mRNA技术从对抗新冠病毒的战场,正式向人类最顽固的敌人-癌症,发起了总攻。
一位结婚近30年的母亲Eileen McGill Fox,在得知丈夫不忠后前往诊所检查,却意外发现自己感染了高危型HPV病毒,随后接连被诊断出外阴癌、宫颈癌和肛门癌,本可以通过一剂早在2006年就已问世的HPV疫苗来预防。
2026年3月24日,恒赛生物宣布,其自主研发的原创树突状细胞疫苗(DC疫苗)KSD-101注射液,正式获得美国食品药品监督管理局(FDA)授予的再生医学先进疗法(RMAT)认定,用于治疗复发或难治性EBV阳性淋巴瘤。这不仅是该产品继2025年底获得FDA快速通道资格后的又一里程碑,更标志着中国在个体化癌症疫苗赛道上,...
2021年10月19日,46岁的护士Jennifer Davis接受了一剂特殊的注射。她是全球首位接受这款三阴性乳腺癌预防疫苗的人。这三年前,她被诊断出患有这种最具侵袭性、复发率高达40%的乳腺癌亚型。历经误诊、化疗副作用危及生命、双乳切除术和26轮放疗后,她虽已“无癌”,却始终活在复发的恐惧中,“每次头痛都让我心惊胆...
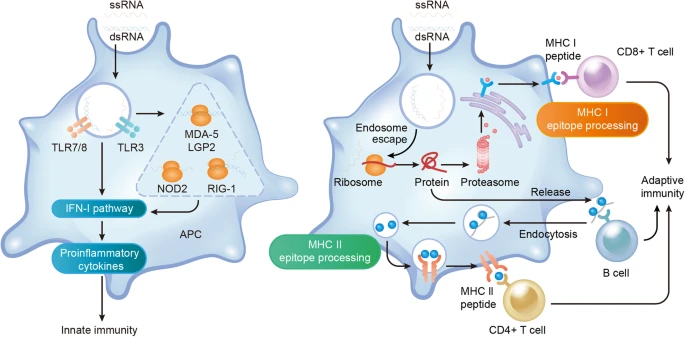
近年来,一种因新冠疫情而广为人知的技术-mRNA疫苗,正以其独特的机制和令人振奋的早期数据,为癌症治疗绘制出一幅充满希望的新蓝图。
近日,国家药品监督管理局药品审评中心(CDE)显示:恒赛生物KSD-101注射液临床试验获得批准,适应症为“经标准治疗无效的EBV相关血液肿瘤”,标志着中国首个获得美国FDA IND批件、中国首个获得FDA快速通道资格(FTD)认定的原创树突细胞疫苗(DC疫苗)产品正式进入国内临床试验阶段。