
7月25日,《Cancer Immunology Research》刊登了一篇题为“Machine Learning–Directed Conversion of Glioblastoma Cells to Dendritic Cell–like Antigen-Presenting Cells as Cancer Immunotherapy”的研究论文,文中报告了一项由AI技术将癌细胞转化为树突状细胞(DC)来识别癌细胞并指挥其他免疫细胞杀死肿瘤细胞的研究结果。

参考资料 1.https://aacrjournals.org/cancerimmunolres/article-abstract/doi/10.1158/2326-6066.CIR-23-0721/746681/Machine-Learning-Directed-Conversion-of?redirectedFrom=fulltext 2.https://www.diakonosoncology.com/wp-content/uploads/2024/04/DIAKONS_AACR-poster-2024-final.pdf 3.https://www.diakonosoncology.com/news/diakonos-oncologys-unique-dendritic-cell-vaccine-doc1021-improves-survival-compared-to-standard-of-care-in-phase-1-trial-for-glioblastoma/ 4.https://ascopubs.org/doi/10.1200/JCO.23.02585 5.https://www.nature.com/articles/s41698-022-00279-3 6.https://ascopubs.org/doi/10.1200/JCO.2024.42.16_suppl.2545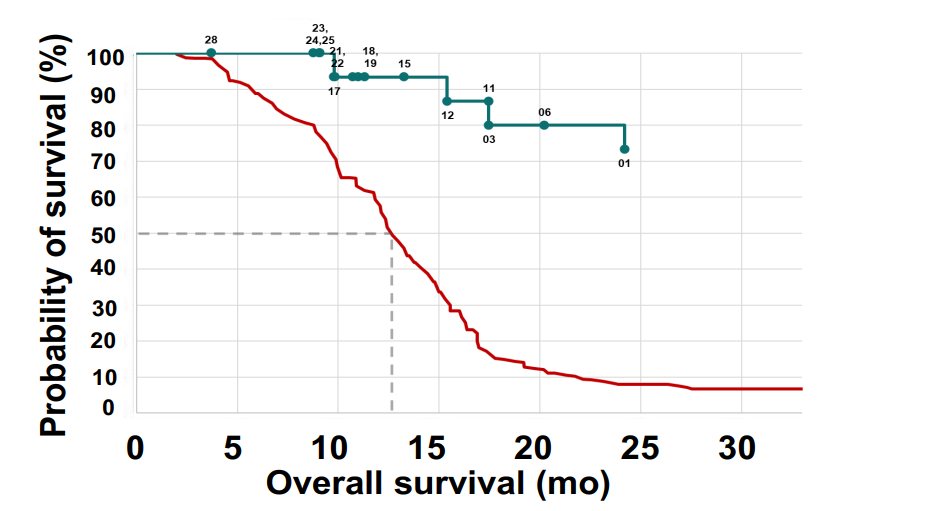






相关推荐
随便看看
- 突破口!MASCT-I(DC+T序贯治疗)打破无药可用的困境,小癌种膀胱癌的新选择!
- 5年总生存率达75%!DC疫苗在白血病、肝细胞癌、非小细胞肺癌中显奇效
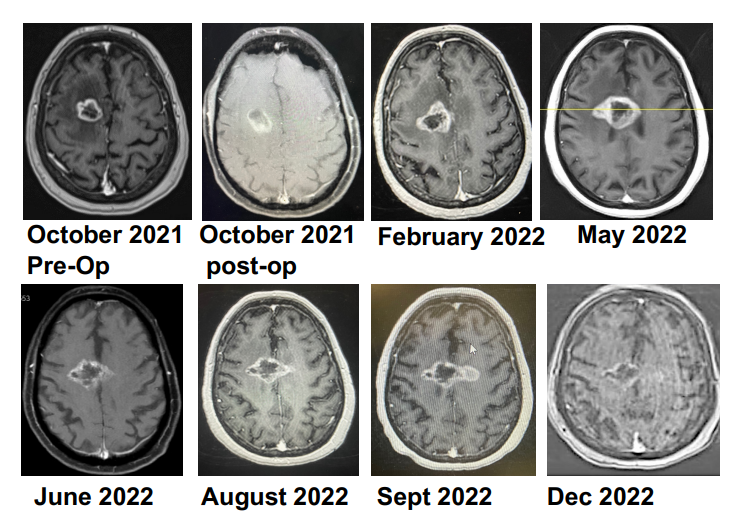
- 自体树突状细胞(DC)疫苗 DOC1021 实现胶质母细胞瘤患者1年生存率达到 93%
- 完全消失!DC疫苗剑指胶质母细胞瘤、胰腺癌、胃癌、尿路上皮癌
- 无进展生存期超577天!肿瘤疫苗为肿瘤患者带来曙光,DC疫苗重拳出击!
- DC疫苗:一位去世的诺奖得主留下的生命礼物,将胰腺癌生存期延长12倍
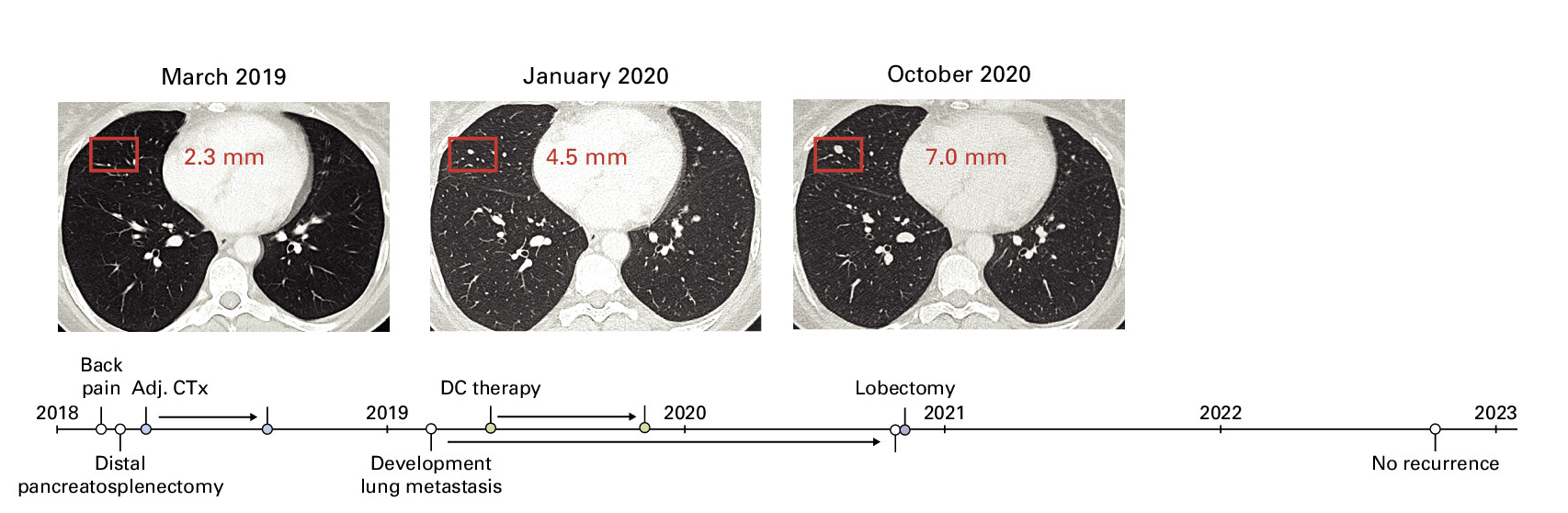
- 2年未复发!哪些癌症适合树突状细胞(DC)疫苗?肿瘤患者迎来全新生机!
- 详细了解DC疫苗
- 树突状细胞(DC)疫苗DOC1021治疗胶质母细胞瘤
- 疾病控制率达75%!树突状细胞(DC)疫苗重锤前列腺癌、肺癌、胶质母细胞瘤等











