2024年2月19日,《Nature》发表了瑞戈非尼联合纳武利尤单抗治疗不可切除的肝细胞癌(uHCC)患者的II期RENOBATE 试验数据。

共有42例患者接受治疗,结果显示:客观缓解率(ORR)为 31.0%,其中1例患者实现完全缓解(CR),12例患者实现部分缓解(PR),21例患者病情稳定(SD),中位缓解持续时间(DOR)为 10.3 个月。

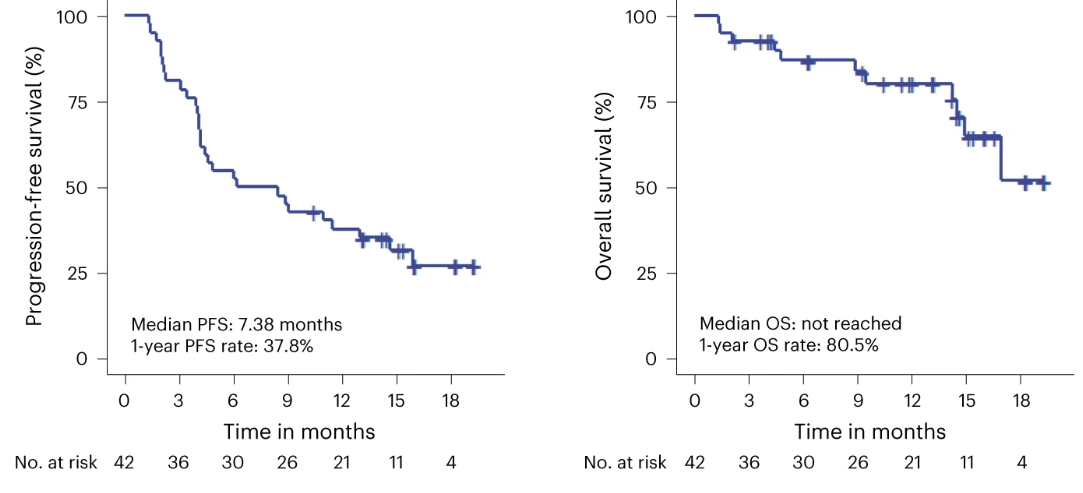
中位无进展生存期(PFS)为 7.38 个月,1年无进展生存率为 37.8%,未达到中位总生存期(OS),1年生存率(OS)为 80.5% 。
8例患者出现不良事件,2例患者出现掌跖红觉不良综合征,蛋白尿、全身无力、胰腺炎、皮疹、血小板计数减少和血清胆红素升高各1例患者。
该试验表明,瑞戈非尼联合纳武利尤单抗具有临床活性,是不可切除的肝细胞癌(uHCC)患者耐受性良好的一线治疗。
肝癌是我国最常见的恶性肿瘤之一,2022年中国肝癌新发病例数约为36.77万,
近年来,免疫治疗的快速发展改写了晚期肝癌的治疗格局,尤其是靶免联合治疗方案已成为晚期肝细胞癌的重要一线治疗模式。肝细胞癌(HCC)是最常见的肝癌形式,占病例的90%。乙型肝炎病毒(HBV)感染是 HCC 发展的最突出危险因素,占病例的50%。
目前针对肝癌的临床试验正在全国范围内寻找患者,患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。如果有需要或有兴趣了解临床试验的患者可以咨询康和源免疫之家医学部(400-880-3716)。
项目名称:SCG101治疗乙型肝炎病毒相关肝细胞癌的I期临床研究
部分入选标准:1.年龄18-70周岁;
2.晚期肝细胞癌患者;
3.有一个可测量靶病灶;
4.预计生存期≥3个月。
临床试验对于传统疗法无效或疗效较差的患者来说,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家医学部(400-880-3716)来寻找适合的临床研究。
参考资料
https://www.esmo.org/oncology-news/activity-and-safety-of-regorafenib-plus-nivolumab-in-first-line-treatment-for-patients-with-unresectable-hepatocellular-carcinoma












