相关推荐
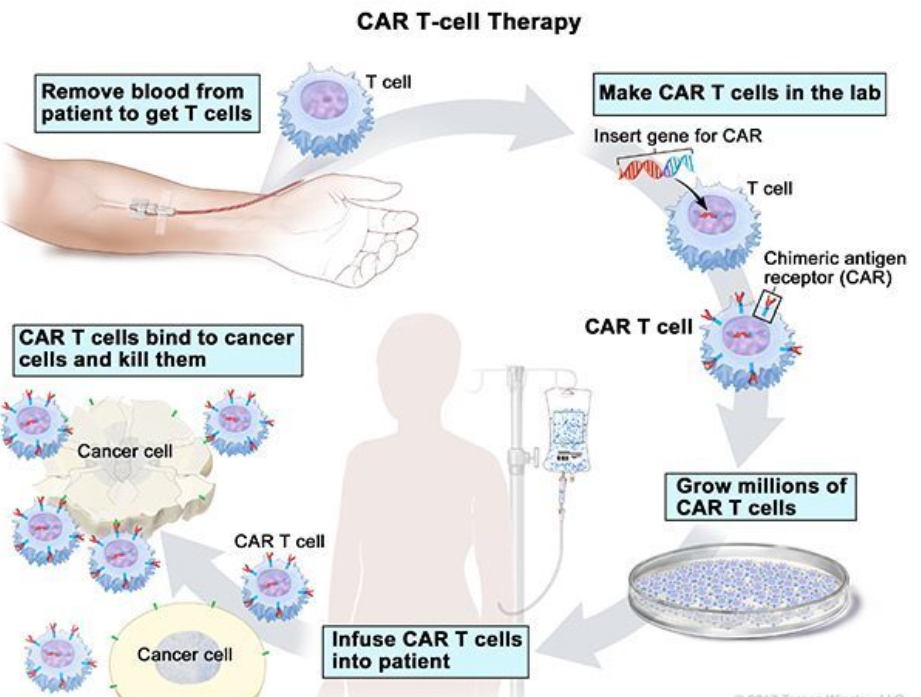
无癌生存超5年、100%缓解!CAR-T疗法交出惊人答卷,为癌症患者带来长期生存希望
当首位接受CAR-T细胞治疗的白血病儿童艾米莉·怀特(Emily Whitehead)成功实现完全缓解(CR)时,CAR-T细胞治疗以前所未有的革命性姿态宣布了癌症治疗新时代的到来,这一成功进一步加速了2017年全球首款CAR-T药物Kymriah的获批上市,开启了癌症免疫治疗的新时代。
免疫管家 2025-09-23

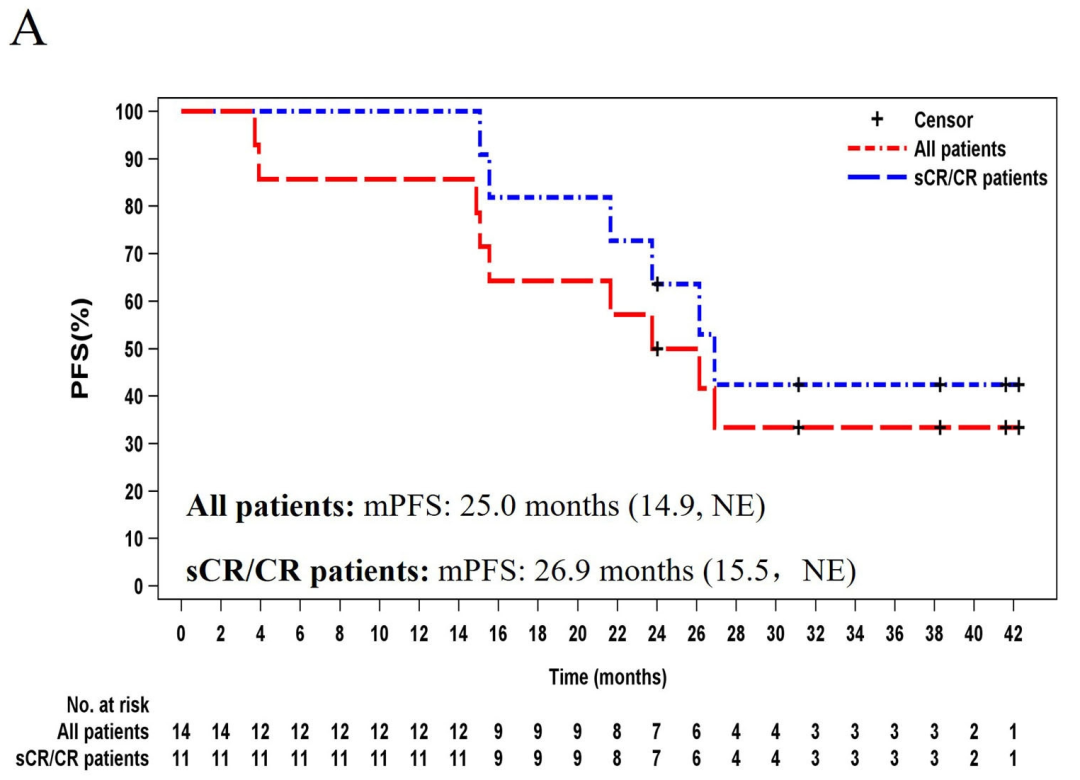
泽沃基奥仑赛注射液用于多发性骨髓瘤的长期随访更新结果亮相2025年IMS年会
9月18日,科济药业宣布,赛恺泽®(泽沃基奥仑赛注射液)用于复发/难治性多发性骨髓瘤患者的I期临床试验的长期随访更新结果,已在第22届国际骨髓瘤学会(IMS)年会上展示。
免疫管家 2025-09-18

生存期超4.5年!CAR-T疗法为骨髓瘤患者带来深度缓解与长期生存希望,92%患者肿瘤缩小或消失!
长期以来,癌症一直是人类健康的重大威胁,给无数患者及其家庭带来了沉重的打击。然而,医学的进步从未停止,嵌合抗原受体T细胞(CAR-T)疗法的出现为癌症患者带来了新的希望。
免疫管家 2025-09-16
100%缓解率!中国CAR-T疗法登上国际舞台,让晚期癌症患者肿瘤完全消失!
在人类与癌症的持久战中,每一次医学突破都像黑暗中的一盏明灯,给无数患者带来了生存的希望。近年来,CAR-T疗法已成为癌症治疗领域一颗耀眼的明星,以其显著的疗效吸引了全球医学界和患者的关注。
免疫管家 2025-06-17

靶向GPRC5D的自体CAR-T细胞产品-CT071用于治疗新诊断的多发性骨髓瘤临床结果亮相2025 EHA
2025 年欧洲血液学协会年会(EHA)年会于2025年6月12日至15日在意大利米兰盛大举行。EHA 是欧洲乃至全球血液学领域最具影响力的学术会议之一,每年都会吸引来自世界各地的血液学专家、研究人员、临床医生和行业代表参加。会议内容包括最新的血液学研究进展、临床试验结果、治疗指南更新、技术创新等,是血液学领域交流和展...
免疫管家 2025-06-16

靶向GPRC5D的自体CAR-T细胞产品CT071研究成果即将亮相2025年EHA年会
2025年4月29日,科济药业宣布其CT071(一种靶向GPRC5D的自体CAR-T细胞产品)用于治疗新诊断的多发性骨髓瘤(NDMM)的研究者发起的临床试验(NCT06407947)的研究结果摘要已被2025年欧洲血液学协会(EHA)年会接受,将在壁报展示环节进行发布。
免疫管家 2025-04-29

超90%的缓解率!国产CAR-T细胞疗法拯救晚期多发性骨髓瘤、淋巴瘤、白血病患者
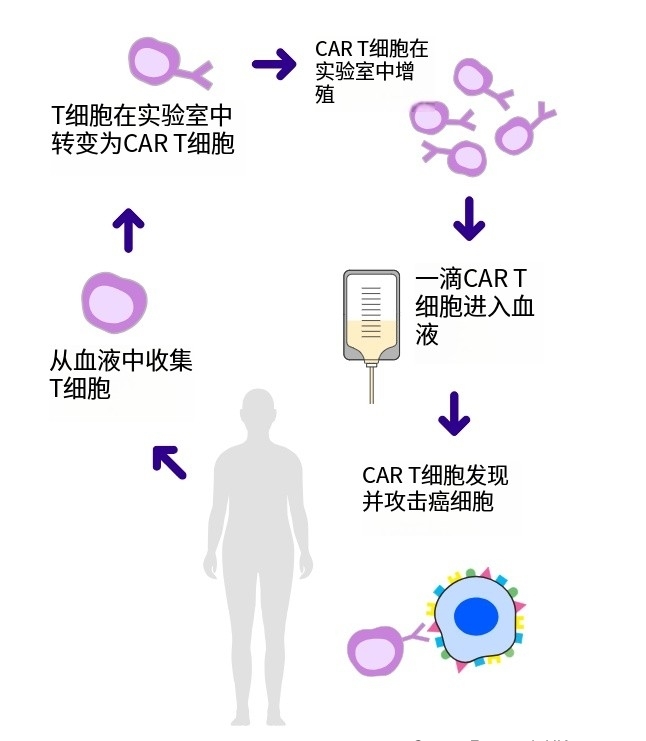
CAR-T细胞疗法的出现犹如一道划破夜空的闪电,为晚期癌症患者带来了新的希望。这种革命性的治疗方法,通过将T细胞取出体外,给T细胞安装上能够精准识别癌细胞的“导航”,并增殖、活化T细胞,让T细胞变得更强,并将增强后的T细胞回输至患者体内,以此来帮助T细胞战胜癌细胞。
免疫管家 2025-03-18

惊爆!国内外CAR-T细胞疗法在癌症治疗领域“狂飙”,骨髓瘤、白血病、淋巴瘤患者的“救命稻草”!
近日,科济药业开发的通用型BCMA CAR-T实现首例入组多发性骨髓瘤患者达到严格意义上的完全缓解(sCR)和微小残留病(MRD)阴性。
免疫管家 2025-03-04
超九成患者病情得到控制!国研CAR-T细胞产品“火力全开”,横扫结直肠癌、肝癌、骨髓瘤、淋巴瘤
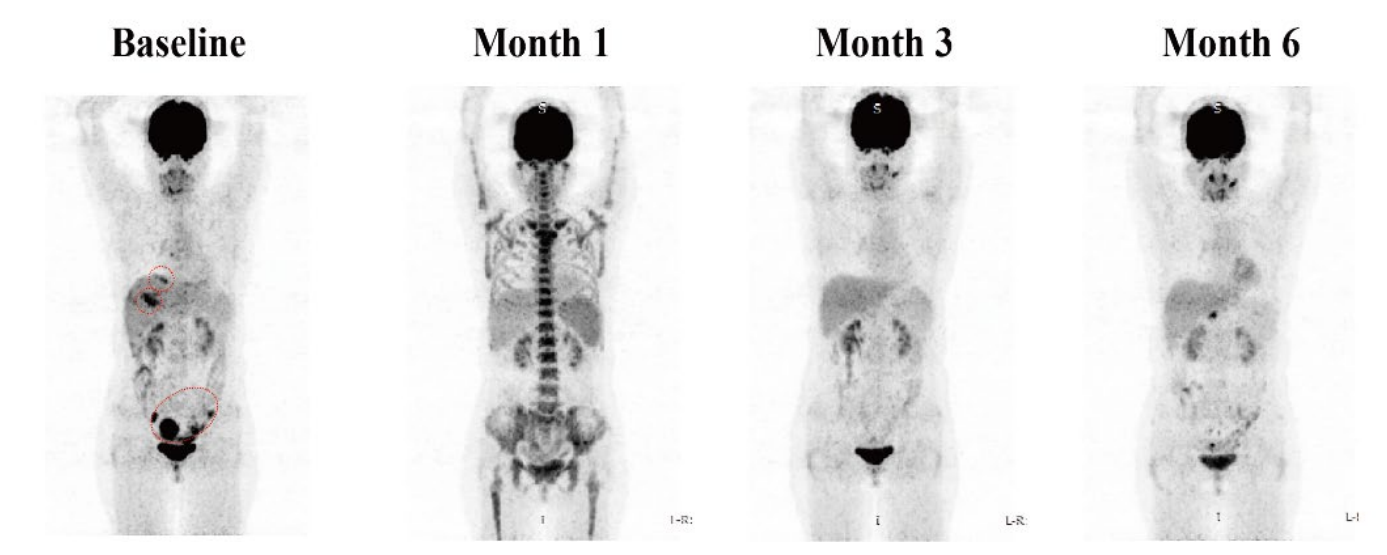
近日,国内科济药业通用型BCMA CAR-T产品首例入组患者在第28天疗效评估时,取得积极的疗效。 据介绍,该患者是一名复发/难治性多发性骨髓瘤患者,既往曾经接受过3线联合药物治疗和自体造血干细胞移植,疾病进展后入组临床试验。经CAR-T治疗后达到严格意义上的完全缓解(sCR),且微小残留病灶(MRD)阴性。 ...
免疫管家 2025-02-12

超九成患者产生临床反应!CAR-T细胞疗法攻克多发性骨髓瘤
2024年美国血液学会(ASH)年会将在12月份在美国圣地哥亚举行,美国血液学会年会(ASH年会)是全球首屈一指的血液学领域的科学交流盛会。此次会议上将公布众多CAR-T细胞治疗产品在多发性骨髓瘤中的最新研究数据。下面小编带大家抢先了解几项CAR-T细胞产品亮眼的临床数据。
免疫管家 2024-11-07