2025年3月26日,美国食品药品监督管理局批准卡博替尼(Cabometyx)用于 12 岁及以上患有既往接受过治疗的、不可切除的局部晚期或转移性、高分化胰腺神经内分泌瘤(pNET)和高分化胰腺外神经内分泌瘤(epNET)的成人和儿童患者。

卡博替尼(Cabometyx)是由美国生物制药公司Exelixis研发的一款口服小分子酪氨酸激酶抑制剂(TKI)。
2024年9月,《新英格兰医学杂志》发表了卡博替尼治疗晚期神经内分泌肿瘤的 3 期试验结果。
共有 203 例患者被随机分配到胰腺外神经内分泌肿瘤队列,95 例患者被分配到胰腺神经内分泌肿瘤队列。
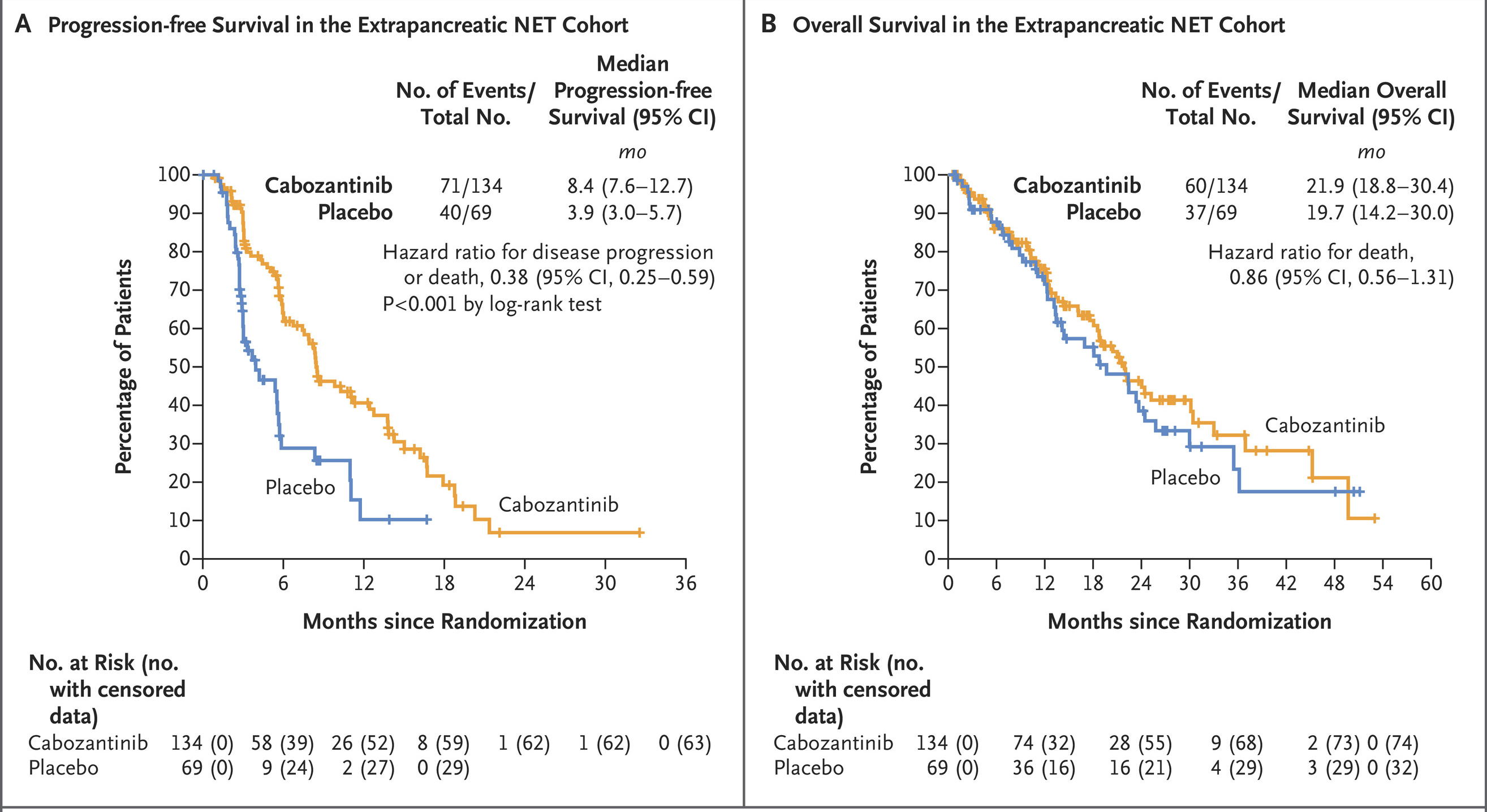
在胰腺外神经内分泌肿瘤队列的 203 例患者中,与安慰剂相比,卡博替尼的疾病进展或死亡风险平均降低了 62%。卡博替尼组的中位无进展生存期为 8.4 个月,安慰剂组为 3.9 个月。卡博替尼组7例患者部分缓解(PR),87例患者病情稳定(SD),在卡博替尼组和安慰剂组分别有 67% 和 29% 的患者观察到靶病灶的减少。安慰剂组37例患者病情稳定(SD)。卡博替尼组的中位总生存期为 21.9 个月,安慰剂组为 19.7 个月。
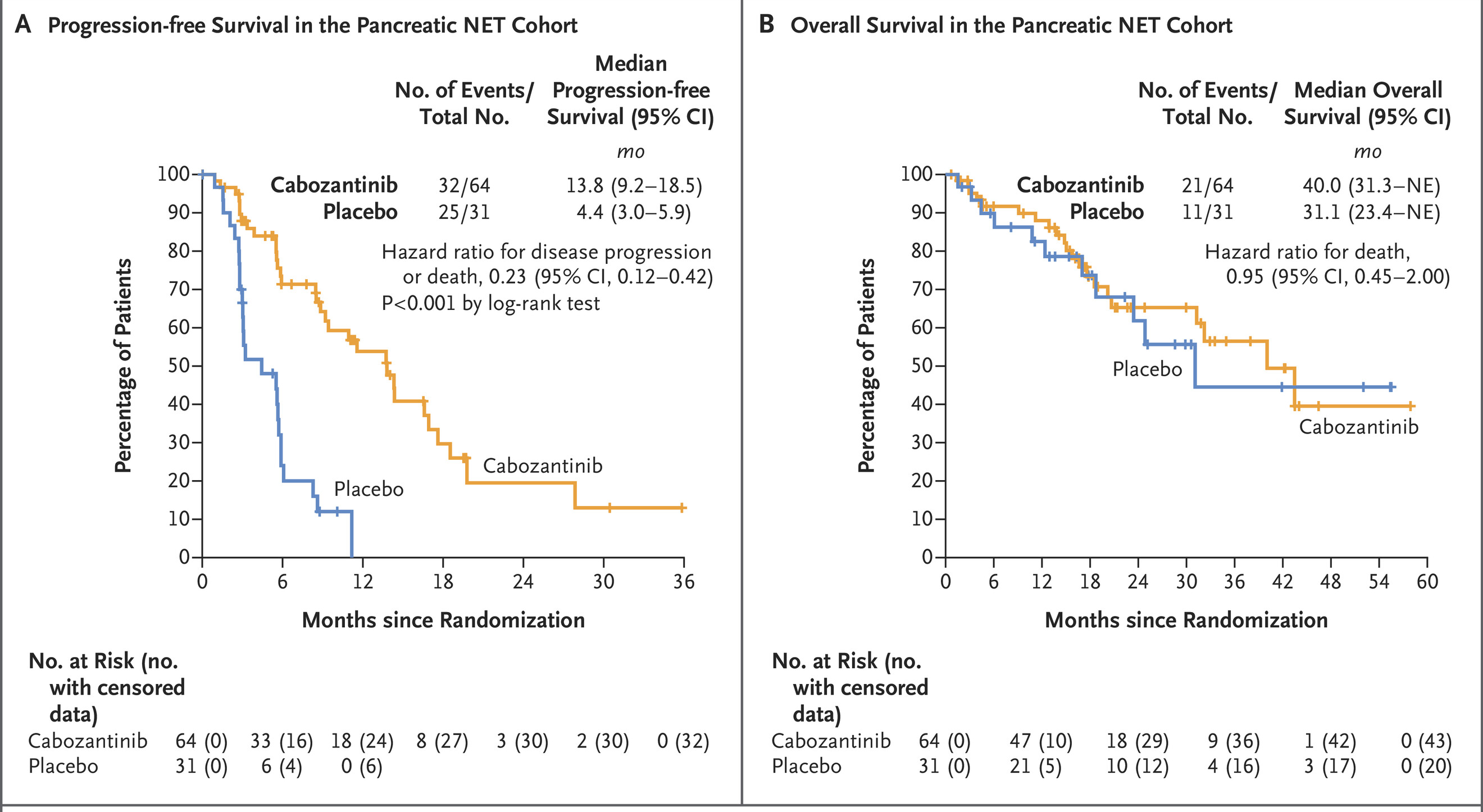
在胰腺神经内分泌肿瘤队列的 95 例患者中,12例患者部分缓解(PR),39例患者病情稳定(SD),安慰剂组仅17例患者病情稳定(SD)。与安慰剂相比,卡博替尼的疾病进展或死亡风险平均降低 77%。卡博替尼组的中位无进展生存期为 13.8 个月,安慰剂组为 4.4 个月,在卡博替尼组和安慰剂组的 80% 和 24% 的患者中分别观察到靶病灶的减少。卡博替尼组的中位总生存期为 40.0 个月,安慰剂组为 31.1 个月。
临床试验对于传统疗法无效或疗效较差的患者来说,是寻找新的治疗药物和方法最快最安全的途径,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。目前有临床试验正在寻找患者,患者可通过参加临床试验来接受药物治疗,年龄、疾病类型和阶段、药物史情况等符合临床试验“入选标准”的患者方可免费入组接受治疗。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家(400-880-3716)来寻找适合的临床研究。
https://www.nejm.org/doi/full/10.1056/NEJMoa2403991

相关推荐
随便看看
- 明济生物M108单抗注射液拟纳入突破性治疗
- ADC药物DB-1419、DB-1303(BNT323)在实体瘤中显威
- 依沃西单药对比帕博利珠单抗单药一线治疗非小细胞肺癌的III期HARMONi-2研究亮相WCLC
- 美国FDA批准cosibelimab用于皮肤鳞状细胞癌
- HL-085联合维莫非尼的治疗方案为BRAF V600E突变的实体瘤患者带来曙光
- Garsorasib 格舒瑞昔 (D-1553)
- 百济神州三款血液肿瘤治疗产品最新数据亮相2025 EHA
- 结直肠癌首个国产EGFR单克隆抗体药物-西妥昔单抗β注射液获批上市
- 欧盟委员会批准埃万妥单抗联合化疗用于治疗非小细胞肺癌
- 疾病控制率高达92.0%!赛沃替尼新适应症上市申请已获国家药监局受理











