相关推荐

ADC药物7MW3711最新进展即将亮相2025 ESMO
近日,迈威生物宣布将于 2025 欧洲肿瘤内科学会(ESMO)大会以壁报形式展示的靶向 B7-H3 ADC 创新药 7MW3711 用于多种晚期实体瘤的 I/II 期临床研究数据及最新进展。
免疫管家 2025-10-14

疾病进展风险降低70%!国产ADC明星药芦康沙妥珠单抗获批第三适应症,抗癌前景广阔
10月11日,国家药品监督管理局(NMPA)批准芦康沙妥珠单抗用于治疗经表皮生长因子受体(EGFR)酪氨酸激酶抑制剂(TKI)治疗后进展的EGFR基因突变阳性的局部晚期或转移性非鳞状非小细胞肺癌(NSCLC)成人患者,这是芦康沙妥珠单抗在国内获批的第三项适应症。
免疫管家 2025-10-14
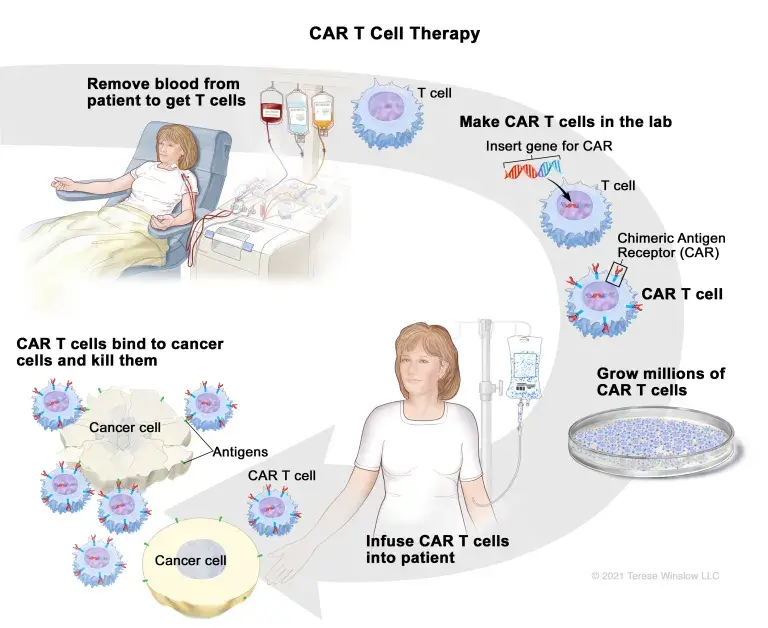
96.3%的缓解率!CAR-T细胞疗法显示强劲疗效,为淋巴瘤、骨髓瘤患者带来长期生存希望
过去十年间,免疫疗法在癌症治疗领域取得了巨大进展,凭借其近年来的临床成功,免疫疗法已成为癌症治疗的常见治疗选择之一。目前,正在研究中的癌症免疫疗法策略众多,包括免疫检查点抑制剂、癌症疫苗、细胞免疫疗法等。嵌合抗原受体(CAR)-T细胞疗法是癌症免疫治疗领域中一个令人兴奋且前景广阔的方向,在某些血液系统恶性肿瘤中已显示出...
免疫管家 2025-10-14
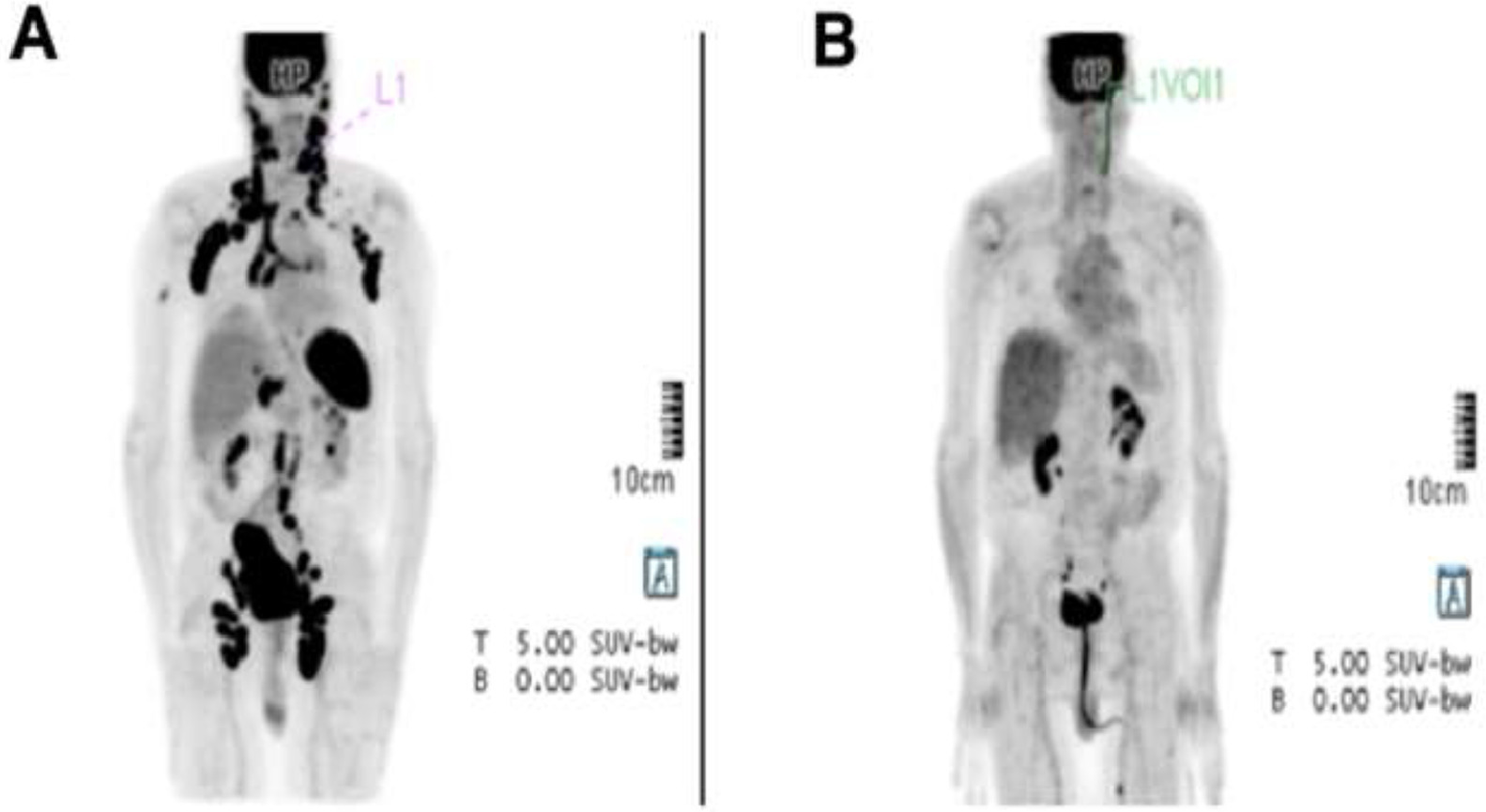
CD5靶向CAR-T细胞治疗复发/难治性T细胞淋巴瘤I期研究结果
2020年3月,贝勒医学院细胞和基因治疗中心研究人员描述了一项针对复发或难治性(r/r)T细胞恶性肿瘤的自体CD5靶向CAR-T细胞的I期剂量递增研究(NCT03081910)。
免疫管家 2025-10-11
德曲妥珠单抗较恩美曲妥珠单抗显示出更高统计学显著性和临床意义的无浸润性疾病生存期改善
9月30日,第一三共宣称德曲妥珠单抗与恩美曲妥珠单抗(T-DM1)相比,在无浸润性疾病生存期(IDFS)方面显示出具有高度统计学差异及临床意义的改善。
免疫管家 2025-10-10

普灵生物 ADC药物PLB-002临床试验申请获得美国FDA批准
近日,普灵生物宣布其首条研发管线PLB-002(抗Claudin6 ADC)的临床试验申请获得美国食品药品监督管理局(FDA)批准。
免疫管家 2025-10-10
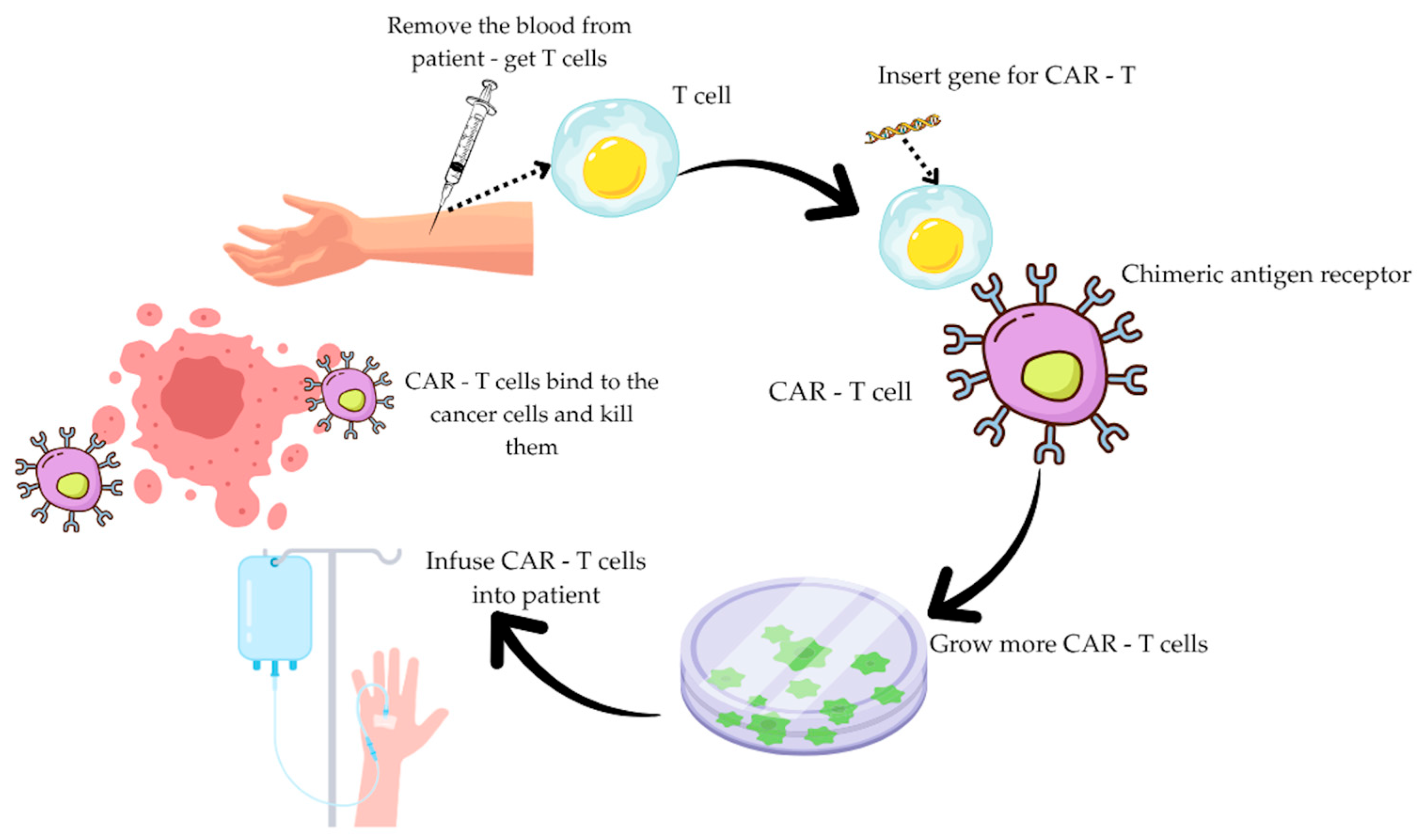
44周完全缓解!国产CAR-T疗法在胃癌、胰腺癌领域连传捷报,为实体瘤患者带来治愈曙光
CAR-T细胞治疗是一种使用患者自身T细胞来对抗癌症的免疫疗法。T细胞在免疫系统中发挥着至关重要的作用,是人体抵御感染和疾病的防御手段。
免疫管家 2025-09-30

美国FDA授予优替德隆孤儿药资格认定
9月25日,华昊中天宣布,其核心产品优替德隆再次被美国食品药品监督管理局(FDA)授予孤儿药资格认定,适应症为胰腺癌。这是继乳腺癌脑转移和胃癌之后,优替德隆被FDA授予的第三项孤儿药资格。
免疫管家 2025-09-29

美国FDA授予raludotatug deruxtecan(R-DXd)突破性疗法认定
9月15日,美国食品药品监督管理局(FDA)已授予raludotatug deruxtecan(R-DXd)突破性疗法认定,用于治疗表达CDH6的铂类耐药上皮性卵巢癌、原发性腹膜癌或输卵管癌的成年患者,这些患者此前曾接受过贝伐珠单抗(bevacizumab)治疗。
免疫管家 2025-09-26

















