6月26日,科济药业宣布,中国国家药品监督管理局(NMPA)已受理舒瑞基奥仑赛注射液(产品编号:CT041,一种靶向Claudin18.2的自体CAR-T细胞产品)的新药上市申请(NDA),用于治疗Claudin18.2表达阳性、至少二线治疗失败的晚期胃/食管胃结合部腺癌(G/GEJA)患者。

舒瑞基奥仑赛注射液是一款潜在全球同类首创的、靶向Claudin18.2蛋白的自体CAR-T细胞治疗候选产品,用于治疗Claudin18.2阳性实体瘤,主要治疗胃/食管胃结合部腺癌及胰腺癌。
此次提交的NDA主要是基于一项在中国开展的开放标签、多中心、随机对照的确证性II期临床试验(CT041-ST-01, NCT04581473)结果。相关数据已在《The Lancet》和2025年美国临床肿瘤学会(ASCO)年会上正式公布。
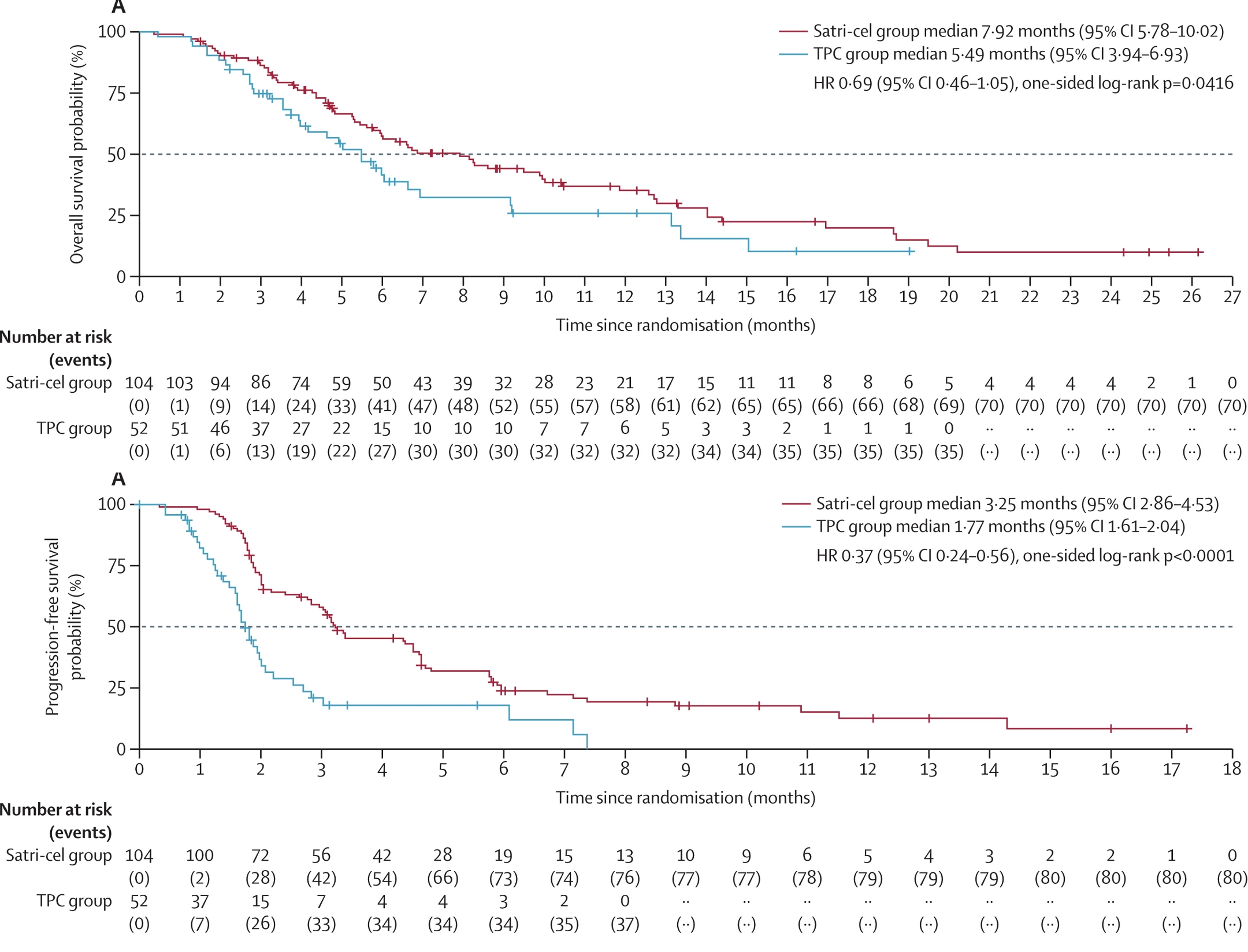
这项临床研究有88例既往接受过治疗的晚期胃癌或胃食管结合部腺癌患者接受舒瑞基奥仑赛注射液治疗,48例患者接受医生选择的治疗。结果显示:舒瑞基奥仑赛注射液组23例患者肿瘤缩小,42例患者病情稳定(SD),疾病控制率(DCR)为65%,中位缓解持续时间(DOR)为5.52个月,中位无进展生存期(PFS)为3.25个月,中位总生存期(OS)为7.92个月。
对照组2例患者肿瘤缩小,持续时间分别为 4.47 个月和 5.42 个月,11例患者病情稳定(SD),疾病控制率(DCR)为25%,中位缓解持续时间(DOR)为4.94个月,中位无进展生存期(PFS)为1.77个月,中位总生存期(OS)为5.49个月。
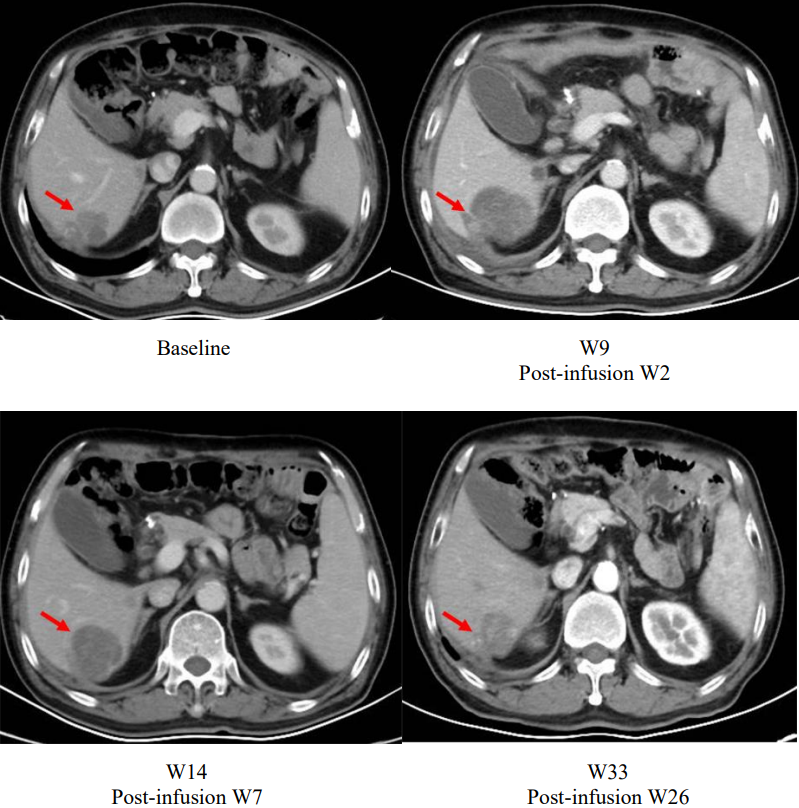
一名患者在舒瑞基奥仑赛注射液输注后第2周,肝脏病变大于基线。病变逐渐在随后的观察中缩小,在输注后第26周小于基线。
目前CAR-T细胞疗法有临床试验正在寻找患者,临床试验对于传统疗法无效或疗效较差的患者来说,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。如果有需要或有兴趣了解临床试验的患者可以咨询康和源免疫之家医学部(400-880-3716)。

相关推荐
随便看看
- PA3-17新适应症临床试验申请获批
- 上海细胞自分泌PD1纳米抗体的闪CAR-T细胞药物用于晚期恶性间皮瘤患者的I期临床研究的初步数据亮相2025 ASCO
- CAR-T产品舒瑞基奥仑赛(CT041)针对胃癌II期临床试验完成入组
- FT819 获得 FDA 的再生医学高级疗法 (RMAT) 认定,用于治疗中度至重度系统性红斑狼疮 (SLE)
- 66%缓解率!CAR-T细胞疗法在血癌、实体瘤中显威,让高危癌症患者存活超5年
- 44周完全缓解!国产CAR-T疗法在胃癌、胰腺癌领域连传捷报,为实体瘤患者带来治愈曙光
- 全球首例通用现货型CAR-Vδ1T细胞药物(UTAA06)实体瘤患者给药
- 《Journal of Clinical Oncology》发表ALLO-501 治疗大 B 细胞淋巴瘤的ALPHA2/ALPHA 临床研究结果
- CAR-T治疗有标可依了!国内两项CAR-T细胞治疗团体标准制定,患者治疗安全再添保障
- 自分泌PD-1纳米抗体装甲化双靶向闪CAR-T产品BZE2203在卵巢癌疗效显著











