2月13日,全球顶尖肿瘤学期刊《Journal of Clinical Oncology》发表了题为:同种异体CAR-T细胞产品Cemacabtagene Ansegedleucel/ALLO-501 治疗复发/难治性大 B 细胞淋巴瘤的I期ALPHA2/ALPHA 临床研究结果。

Cemacabtagene Ansegedleucel (cema-cel)是一款靶向CD19的同种异体CAR-T疗法,用于治疗大B细胞淋巴瘤(LBCL)。2022年6月,美国食品和药物管理局(FDA)授予其再生医学高级疗法(RMAT)称号。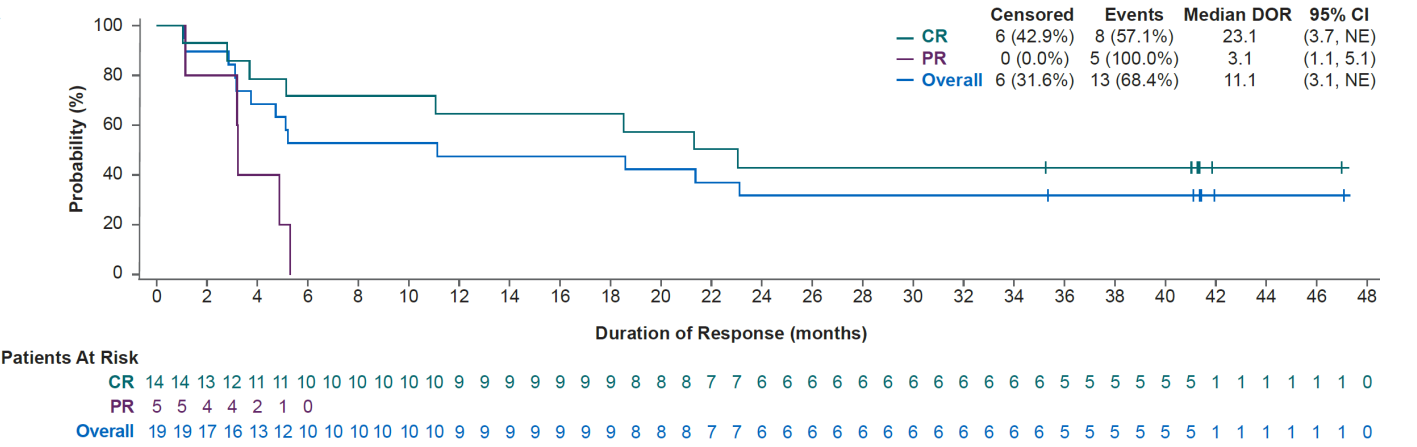

相关推荐
随便看看
- CD7-CAR-T产品PA3-17注射液完全缓解率75%!
- 面对实体瘤这座“堡垒”,CAR-T终于亮剑!胃癌、肝癌、肺癌接连告捷,《自然》研究:我们找到了新的“攻城锤”
- 告别终身服药?CAR-T疗法再封神:不仅治癌,更能跨界到红斑狼疮,让自身免疫病患者长期无药缓解
- CAR-T细胞治疗产品IMC002用的胃癌的I/IIa 期临床研究结果公布于2026 ASCO GI
- 多款CAR-T重拳出击!让更多淋巴瘤,胰腺癌,胃癌,肝癌等患者获益!
- 面对狼疮、硬皮病、肌炎……这一次,CAR-T疗法席卷自免疾病,停药18个月,还能健康生娃
- CAR-T细胞疗法KYV-101重锤重症肌无力、多发性硬化症等自身免疫疾病
- 中位生存近3年!“百万”CAR-T带领淋巴瘤患者走向“治愈”之路
- 无瘤状态超7年!CAR-T细胞疗法突飞猛进,在血液肿瘤与实体瘤治疗中大展身手
- CAR-T细胞疗法让她摆脱了红斑狼疮的折磨,临床症状完全消失











