3月31日,沙砾生物宣布其自主研发的,全球首款膜结合IL-15复合物编辑型肿瘤浸润性淋巴细胞(TIL)疗法GT201成功获得美国食品药品监督管理局(FDA)授予的快速通道认定,用于治疗复发或转移性头颈部鳞状细胞癌(HNSCC)。
GT201注射液是由沙砾生物自主研发的下一代TIL产品,经StaViral®病毒稳转株平台编辑改造后,在TIL细胞表面高表达IL-15。该改造可提高T细胞的肿瘤杀伤功能,并通过促进记忆T细胞的形成,对肿瘤产生更为长效的控制。一系列体外功能试验表明GT201与未经改造的TIL细胞相比,可显著强化TIL的增殖、功能性细胞因子释放和肿瘤杀伤,并在不依赖IL-2或低浓度IL-2的条件下,在体内和体外提升TIL的长期存续和抑瘤效果。GT201目前已在中美两地获批IND,并已进入I期临床研究阶段。
在多种癌症的治疗中展现出了良好的效果。在9例可评估患者中,GT201实现了55.6%的客观缓解率(ORR)和77.8%的疾病控制率(DCR),尤其是在头颈鳞癌和非小细胞肺癌等治疗难度较高的适应症中表现出卓越疗效。
GT201还成功实现了一例晚期头颈鳞癌患者的完全缓解(CR)。该患者为晚期鳞状细胞癌。在化疗未达预期效果后,患者参加了GT201的临床试验。
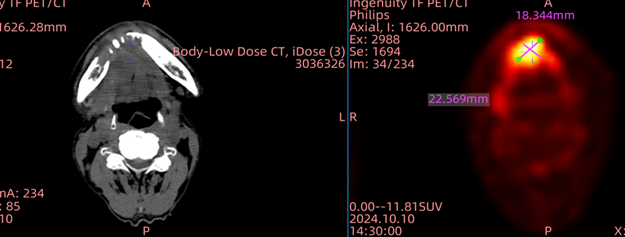
令人欣喜的是,在TIL细胞输注3周后,该患者实现部分缓解(PR),右侧口底、颈部淋巴等多处病灶缩小;9周后所有病灶消失,达到完全缓解(CR)。患者表示,疾病带来的疼痛、吞咽艰难、声音嘶哑等症状逐渐好转,目前“走得动跑得动了,最主要还是吃得动、吃得香了”。
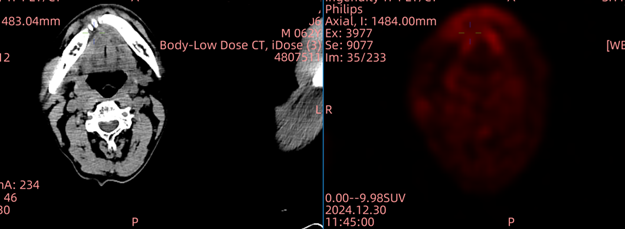
临床试验对于传统疗法无效或疗效较差的患者来说,是寻找新的治疗药物和方法最快最安全的途径,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。目前康和源免疫之家有临床试验正在寻找患者,患者可通过参加临床试验来接受药物治疗,年龄、疾病类型和阶段、药物史情况等符合临床试验“入选标准”的患者方可免费入组接受治疗。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家(400-880-3716)来寻找适合的临床研究。

相关推荐
随便看看
- 持续缓解超1年!TIL细胞疗法瞄准黑色素瘤、肺癌、乳腺癌、宫颈癌、头颈癌、卵巢癌等实体瘤
- 君赛生物GC101 TIL疗法临床捷报:晚期黑色素瘤患者实现部分缓解
- TIL细胞产品GC101在胰腺癌患者中取得积极结果
- 喜讯!TIL疗法lifileucel一线治疗晚期黑色素瘤客观缓解率达 65.2%!
- TIL治疗产品GT307注射液临床试验申请获得美国FDA批准
- 89%生存率!TIL疗法让晚期癌症患者重获生机,41%耐药患者病情获得控制
- TIL细胞产品BST02注射液实现一名晚期肝癌患者靶病灶完全消退
- 癌症克星登场!TIL细胞疗法惠及肺癌、宫颈癌、黑色素瘤……持续缓解超三年
- 美国FDA授予肿瘤浸润淋巴细胞(TIL)疗法OBX-115再生医学高级疗法(RMAT)称号,用于黑色素瘤
- Amtagvi(lifileucel)在加拿大获批上市











