12月4日,美国食品药品监督管理局(FDA)批准Bizengri(zenocutuzumab)上市,适应症为:既往全身治疗期间或之后疾病进展的携带神经调节蛋白 1 (NRG1) 基因融合的晚期、不可切除或转移性非小细胞肺癌(NSCLC)或胰腺癌。

此次获批主要基于eNRGy 试验的数据,该试验招募了 64 名晚期或转移性NRG1融合阳性 NSCLC 成人患者和 30 名晚期或转移性NRG1融合阳性胰腺癌成人患者。结果显示:
NRG1+胰腺癌患者中,客观缓解率(ORR)为 40%,NRG1+非小细胞肺癌患者中,ORR为 33%,中位缓解持续时间(DOR)为 7.4 个月。
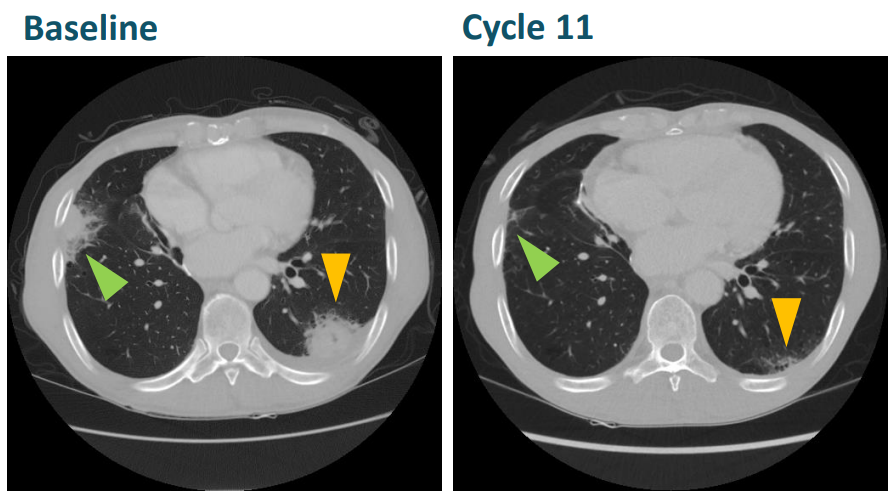
1例65岁非小细胞肺癌患者,伴有肺部和骨转移,既往接受化疗、阿替利珠单抗等治疗,在zenocutuzumab治疗后目标病变缩小53%。
2022年,《Precision Oncology》报告了zenocutuzumab治疗乳腺癌的病例。该患者于 2013 年 4 月被诊断出患有浸润性右乳非粘液性导管癌,2014 年 5 月肝功能恶化后,确诊转移性乳腺癌,于是接受化疗。2014 年 9 月开始接受来曲唑和地诺单抗作为维持治疗,疾病持续缓解持续 2 年。鉴于疾病进展缓慢,患者继续服用来曲唑和地诺单抗 2 年。2018 年 3 月,病情迅速进展,开始了 palbociclib 和氟维司群的联合方案,2019 年 3 月,肝脏出现进展。。开始卡培他滨治疗,患者实现了持续 10 个月的部分代谢反应,直到 2020 年 1 月报告了肝和骨转移的进展。2020 年 7 月参加了zenocutuzumab试验,2个周期后,四个肝脏病灶中观察到完全代谢反应,两个目标肝脏病灶减少了 35%。

临床试验对于传统疗法无效或疗效较差的患者来说,是寻找新的治疗药物和方法的,最快最安全的途径,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。目前有临床试验正在寻找患者,患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家(400-880-3716)来寻找适合的临床研究。
参考资料
1.https://www.fda.gov/drugs/resources-information-approved-drugs/fda-grants-accelerated-approval-zenocutuzumab-zbco-non-small-cell-lung-cancer-and-pancreatic
2.https://merus.nl/wp-content/uploads/2023/12/ESMOASIA2023NRG1NSCLC.pdf
3.https://ascopubs.org/doi/full/10.1200/PO.21.00446

相关推荐
随便看看
- 广泛期小细胞肺癌新药!美国FDA加速批准tarlatamab用于治疗广泛期小细胞肺癌,缓解率达40%!
- 美国食品药品监督管理局(FDA)授予BGB-16673快速通道认定,用于治疗复发/难治性慢性淋巴细胞白血病或小淋巴细胞淋巴瘤患者
- DM005新药临床研究申请获国家药监局批准
- ADC药物Blenrep联合方案获批用于多发性骨髓瘤
- 塞纳帕利单药治疗BRCA1/2突变铂敏感复发性卵巢癌患者的SABRINA研究的最终分析结果亮相2025 ESMO
- ADC药物德曲妥珠单抗(DS-8201,Enhertu,T-Dxd,优赫得)获批胃癌
- 美国FDA授予帕博利珠单抗优先审评
- 富马酸吉瑞替尼片获批
- ADC药物崭露头角,为肺癌、淋巴瘤、乳腺癌、胃癌患者打开生命新通道
- 塞纳帕利用于晚期卵巢癌一线维持治疗的上市许可申请已获得欧洲药品管理局受理











