近日,诺华宣布其创新药物信倍立®(盐酸阿思尼布片)获得国家药品监督管理局批准,用于治疗新诊断的费城染色体阳性的慢性髓细胞白血病(Ph+CML)慢性期(CP)成人患者。这是全球首个且目前唯一获批基于ABL肉豆蔻酰口袋(STAMP)创新机制的靶向药物,为CML患者提供了全新治疗选择。
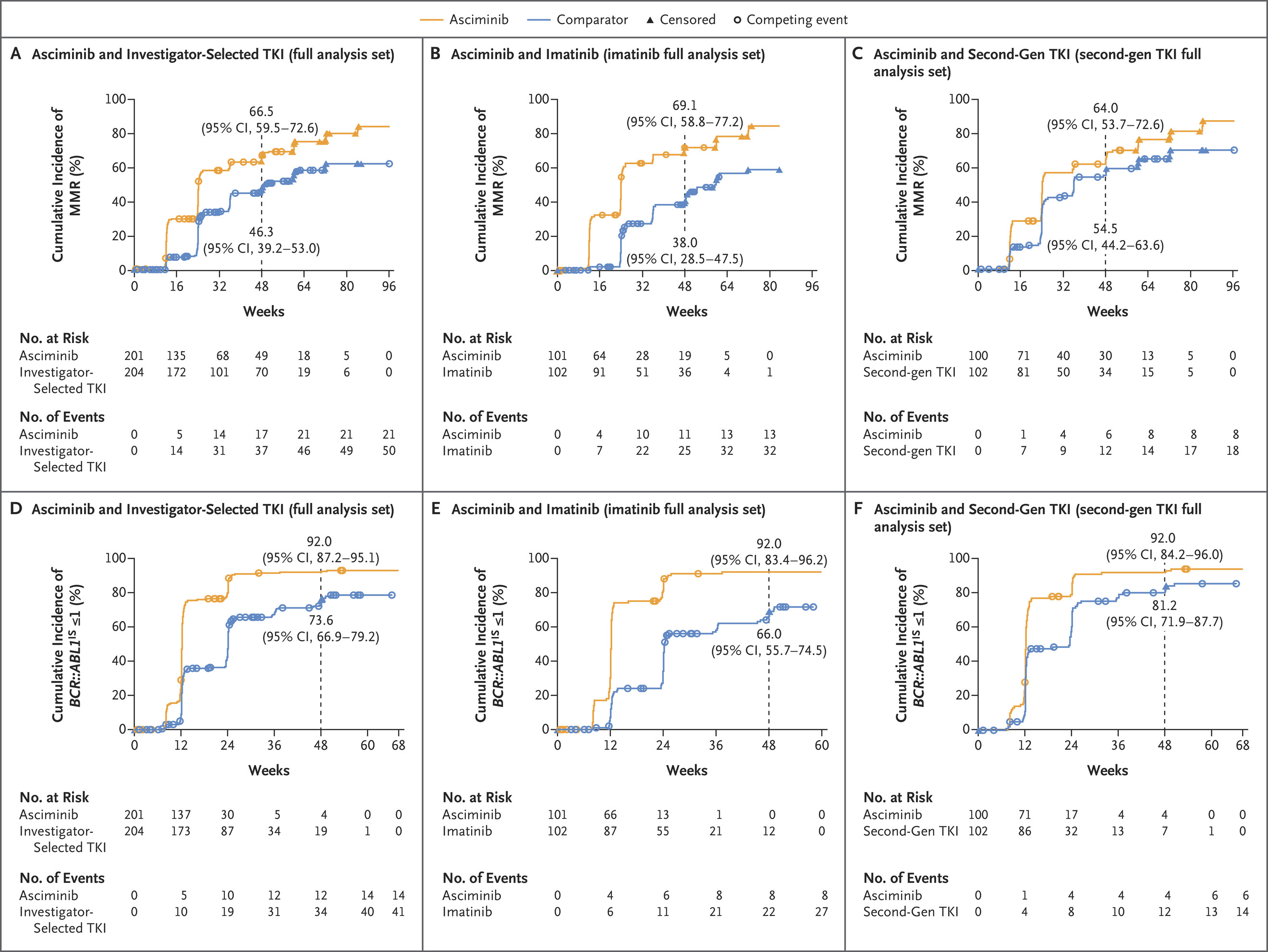
此次获批基于关键性III期ASC4FIRST试验数据,该试验评估了asciminib在新诊断的慢性期费城染色体阳性慢性粒细胞白血病(Ph+ CML)患者中的疗效。共纳入405例患者,201例患者接受asciminib治疗,204例患者接受对照组治疗,结果显示:具有主要分子反应的百分比分别为69.3% 和 40.2%,第48 周时 asciminib 组出现主要分子反应的患者百分比为 66.0%,对照组为57.8%。
阿思尼布(asciminib,ABL001)是针对BCR-ABL1激酶的新型变构抑制剂,采用了与传统TKIs不同的作用机制,结合于靶蛋白的肉豆蔻酰口袋(STAMP)——一种变构位点,通过改变蛋白构象以实现对靶蛋白的抑制。得益于这种独特的机制,阿思尼布表现出更高的选择性,大幅降低脱靶效应,从而减少不良反应,提高患者的耐受性10。
2024年10月29日,美国食品药品监督管理局(FDA)加速批准asciminib(Scemblix)用于新诊断的慢性期费城染色体阳性慢性粒细胞白血病(Ph+ CML)成人患者。
临床试验对于传统疗法无效或疗效较差的患者来说,是寻找新的治疗药物和方法的,最快最安全的途径,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。目前有临床试验正在寻找白血病患者,患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家(400-880-3716)来寻找适合的临床研究。
Andreas Hochhaus, Jianxiang Wang, Dong-Wook Kim, et al.Asciminib in Newly Diagnosed Chronic Myeloid Leukemia.N Engl J Med 2024;391:885-898

相关推荐
随便看看
- 德达博妥单抗用于三阴性乳腺癌的TROPION-Breast02 Ⅲ期临床研究结果亮相2025 ESMO
- 帕博利珠单抗联合方案获美国FDA批准用于HER2阳性胃癌患者
- KPG-818胶囊获批开展临床用于多发性骨髓瘤
- 尿路上皮癌患者新选择!维恩妥尤单抗在国内获批用于治疗尿路上皮癌
- Bcl-2抑制剂APG-2575联合阿扎胞苷治疗急性髓系白血病患者的最新数据公布
- 依沃西联合方案一线治疗晚期胆道癌III期临床完成首例患者入组
- 转载:CAR-T细胞治疗淋巴瘤六年后,患者仍无癌
- SSGJ-707用于晚期非小细胞肺癌患者的研究结果亮相2025 CSCO
- ADC药物JSKN003获美国FDA授予孤儿药资格认定
- 埃万妥单抗联合拉泽替尼一线治疗EGFR突变非小细胞肺癌数据即将在 ELCC 2025 上公布











