9月25日,美国食品药品监督管理局(FDA)批准imlunestrant选择性雌激素受体拮抗剂(SERD)imlunestrant用于治疗既往接受过至少一线内分泌治疗后出现疾病进展的ER+、HER2-、ESR1突变晚期或转移性成人乳腺癌患者。

此次批准主要基于EMBER-3(NCT04975308)研究,该研究纳入了874名ER 阳性、人表皮生长因子受体 2(HER2)阴性晚期乳腺癌患者,其中331名患者接受imlunestrant,330名接受标准治疗,213名患者接受 imlunestront-abemaciclib。结果显示:在ESR1突变患者中,Imlunestrant 治疗组的中位无进展生存期为5.5个月,而标准治疗组为3.8个月。imlunestrant 组估计的 19.4 个月时限制性平均生存时间为 7.9 个月,而标准治疗组为 5.4 个月。所有患者中,imlunestrant 组的中位无进展生存期为5.6个月,标准治疗组的中位无进展生存期为5.5个月。
在ESR1突变患者中,imlunestrant 组18个月时的估计总生存率为77.0%,标准治疗组为58.6%。在所有患者中,imlunestrant 组为78.6%,标准治疗组为71.8%。
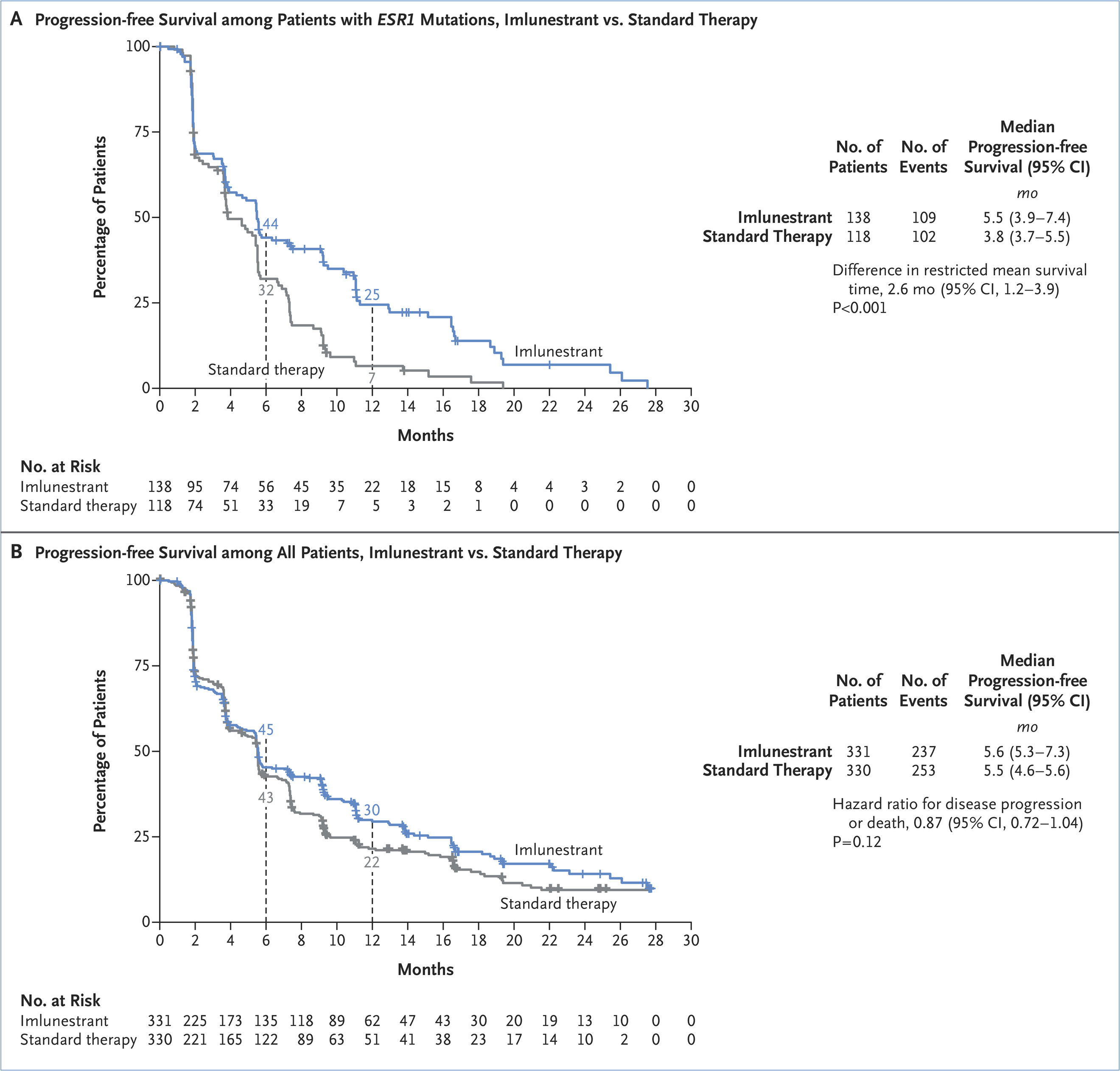
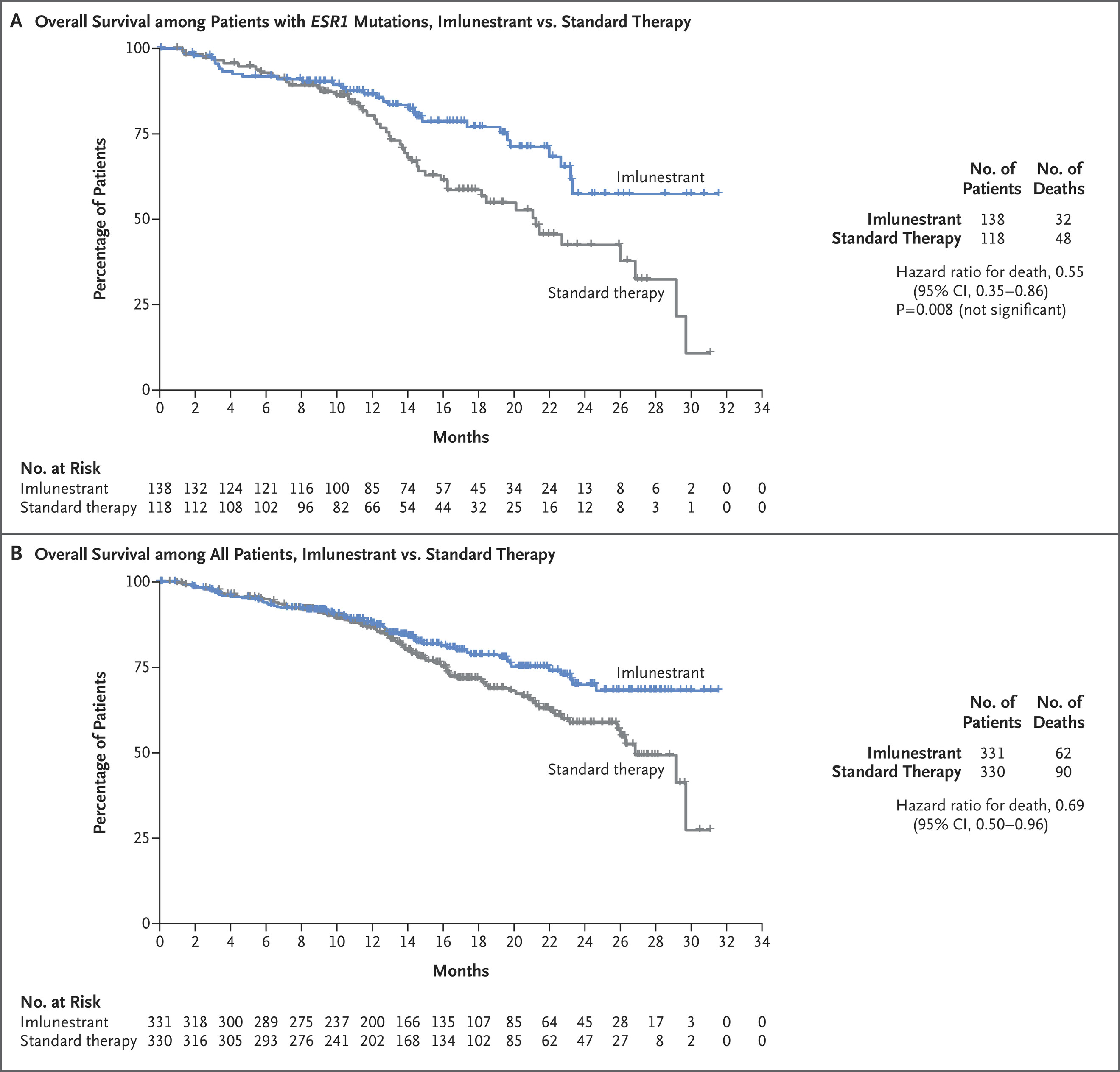
结果表明,在ER阳性、HER2阴性的晚期乳腺癌患者中,在ESR1突变患者中,Imlunestrant治疗的无进展生存期明显长于标准治疗。
临床试验对于传统疗法无效或疗效较差的患者来说,是寻找新的治疗药物和方法的,最快最安全的途径,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。目前有临床试验正在寻找患者,患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家(400-880-3716)来寻找适合的临床研究。

相关推荐
随便看看
- 2025世界肺癌大会公布!德曲妥珠单抗治HER2突变肺癌效果惊人:56.9%患者肿瘤缩小,91.7%病情控制!
- 七倍碾压!上海肿瘤教授发表最新研究成果,放化疗后使用奥希替尼治疗的疾病进展或死亡风险降低84%
- 泰瑞沙(通用名:甲磺酸奥希替尼片以下简称“奥希替尼”)术后辅助治疗适应症成功准入医保目录
- SHR-1701联合结直肠癌的研究结果登上《自然》子刊STTT
- 第四代EGFR抑制剂:BBT-176
- 利厄替尼片用于EGFR T790M突变阳性非小细胞肺癌患者的长期随访数据登2025年 ELCC
- 欧洲药品管理局(EMA)授予KRAS G12C抑制剂戈来雷塞孤儿药疗法认定
- 美国FDA授予靶向HER3的新一代ADC产品DB-1310快速通道资格认定
- PRMT5抑制剂GTA182治疗MTAP缺失晚期非小细胞肺癌的首次人体 I 期临床试验数据亮相ESMO Asia 2025
- 肺癌、淋巴瘤治疗捷报频传!多款ADC新药数据惊艳,疾病控制率高达94.3%











