相关推荐
易慕峰靶向CLDN18.2 CAR-T疗法(IMC002)实现一位晚期转移性胃癌患者完全缓解
7月1日,易慕峰生物公布了其靶向CLDN18.2 CAR-T疗法(IMC002)注册I期临床研究中的一例患者随访观察:一位晚期胃癌并肝转移患者,在首次确认完全缓解(CR)六周后的研究随访中,影像检查显示维持完全缓解状态,且内镜下诊断及胃镜活检呈病理阴性。
免疫管家 2025-07-02

靶向CLDN18.2的ADC药物SKB315联合塔戈利单抗的临床试验申请获批
6月12日,国家药品监督管理局(NMPA)药品审评中心(CDE)显示:科伦博泰申请的靶向CLDN18.2抗体偶联药物(ADC)SKB315联合抗PD-L1单克隆抗体(mAb)塔戈利单抗(科泰莱®)用于一线治疗胃癌/胃食管结合部癌(GC/GEJC)的新药临床试验(IND)申请获得默示许可。
免疫管家 2025-06-12

靶向CLDN18.2单克隆抗体ASKB589在晚期胃/食管胃交界处腺癌二线治疗的最新临床试验数据亮相2025 ASCO
ASKB589是AskGene自主研发的、拥有国际自主知识产权的ADCC增强型第二代抗CLDN18.2人源化单克隆抗体。ASKB589对CLDN18.2的亲和力和特异性高,能转化为更强的抗体依赖细胞介导毒作用(ADCC)和补体依赖的细胞毒性作用(CDC)。拟用于治疗胃/食管胃交界处腺癌患、胰腺癌以及其它有CLDN18....
免疫管家 2025-06-09

靶向Claudin18.2的CAR-T细胞产品舒瑞基奥仑赛注射液(CT041)用于胃/食管胃结合部腺癌患者试验最新数据公布
5月31日,《柳叶刀》发表了科济药业研发的一款靶向Claudin18.2蛋白的自体CAR-T细胞治疗候选产品-舒瑞基奥仑赛注射液(CT041)针对Claudin18.2阳性、至少二线治疗失败的晚期胃/食管胃结合部腺癌患者的II期临床试验(CT041-ST-01, NCT04581473)的研究结果。这是全球首个针对实体...
免疫管家 2025-06-04

胃癌患者生存期延长!CAR-T疗法最新数据震撼发布,已有患者肿瘤显著缩小!
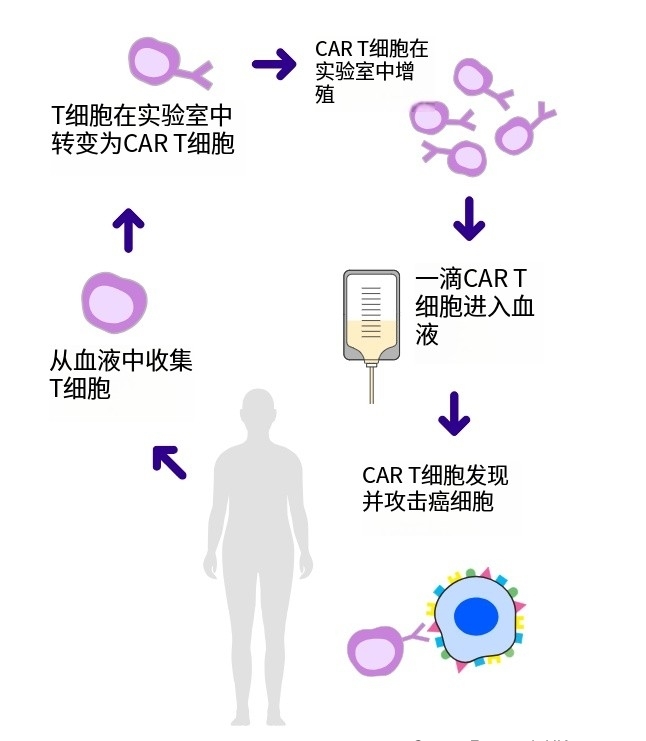
CAR-T疗法,即嵌合抗原受体T细胞疗法,它的工作原理是将你的T细胞转变为更高效的抗癌“机器”。在CAR-T细胞疗法中,医护人员会将一个新基因引入你的T细胞,从而改变这些细胞,使它们能够更有效地检测和杀死癌细胞。简单来说,就是从患者自身的血液中提取T细胞,然后在实验室中对这些T细胞进行基因改造,给它们装上一种特殊的“导...
免疫管家 2025-06-04

舒瑞基奥仑赛注射液(CT041)拟纳入优先审评
5月20日,国家药品监督管理局药品审评中心(CDE)显示:舒瑞基奥仑赛注射液(CT041)拟纳入优先审评,用于治疗CLDN18.2表达阳性、至少二线治疗失败的晚期胃/食管胃结合部腺癌。
免疫管家 2025-05-21

XNW27011拟纳入突破性治疗
5月16日,国家药品监督管理局药品审评中心(CDE)显示:信诺维申请的注射用XNW27011拟纳入突破性治疗,用于CLDN18.2表达的局部晚期不可切除或转移性HER2阴性胃或胃食管结合部腺癌的三线及以上治疗。
免疫管家 2025-05-16

自分泌PD-1纳米抗体装甲化双靶向闪CAR-T产品BZE2203在卵巢癌疗效显著
美国癌症研究协会(AACR)年会是全球肿瘤学领域的顶级盛会,近日,2025年第116届AACR年会在美国芝加哥举行。此次会议上,由上海细胞治疗集团联合上海大学附属孟超肿瘤医院及美国子公司Chantibody(CHANTIBODY THERAPEUTICS INC.)共同开展的一项治疗实体肿瘤的自分泌抗PD-1纳米抗体装...
免疫管家 2025-05-15

54岁卵巢癌患者绝处逢生!CAR-T产品BZE2203在卵巢癌战场创造奇迹
卵巢癌是常见的妇科恶性肿瘤之一,这个看似陌生却又悄然威胁着无数女性生命健康的“沉默杀手”,它的发病率在女性生殖系统肿瘤中位居前列,且死亡率长期居高不下,堪称女性健康的重大隐患。2022年,全球约诊断出32.5万例卵巢癌新发病例,约有20.7万例卵巢癌患者死亡。
免疫管家 2025-05-14

BCMA CAR-T产品CT0596初步临床数据公布
近日,科济药业公布了CAR-T细胞产品CT0596的初步临床数据。CT0596为科济药业基于THANK-u Plus™平台开发的一款靶向BCMA的通用型CAR-T细胞注射液,目前正在复发/难治性多发性骨髓瘤(R/R MM)或复发/难治性浆细胞白血病(R/R PCL)中开展一项早期探索性临床研究,用于评估CT0596的安...
免疫管家 2025-05-12















