相关推荐

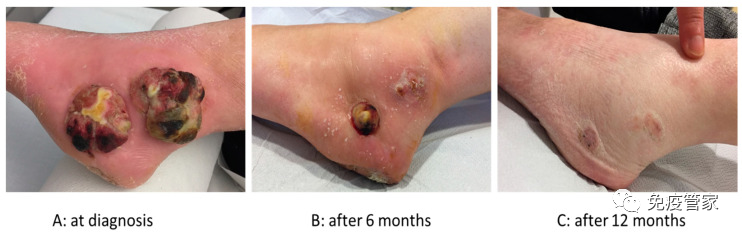
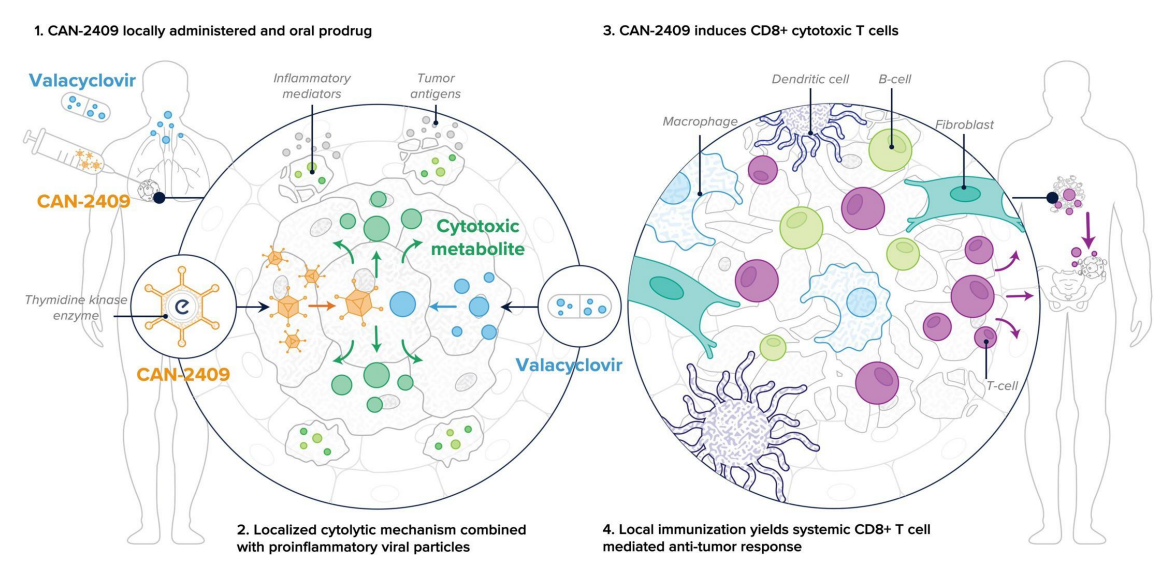
1年肿瘤完全消失!国内研究团队利用溶瘤病毒让晚期癌症患者实现20个月无癌生存
溶瘤病毒并不是一个全新的概念。早在19世纪末,人们就观察到一些癌症患者在感染病毒后,肿瘤竟然出现了缩小的现象。一个多世纪以来,研究人员一直在研究病毒如何成为对抗癌症的工具。直到近年来,随着科学技术的不断进步,溶瘤病毒才逐渐从一个偶然的发现发展成为一种有潜力的抗癌疗法。
免疫管家 2025-07-03

中生复诺健溶瘤病毒产品-VG161用于肝癌的研究成果亮相2025 ASCO
2025年美国临床肿瘤学会(ASCO)年会在芝加哥隆重召开,作为全球最具影响力的肿瘤学盛会,每年都会吸引来自世界各地的顶尖肿瘤专家、学者、科研人员以及药企代表齐聚一堂。在这里,他们分享最新的研究成果、探讨最前沿的治疗理念,共同推动肿瘤治疗技术的不断进步。此次会议上公布了多项突破性研究。其中,中生复诺健公布了其溶瘤病毒产...
免疫管家 2025-06-18
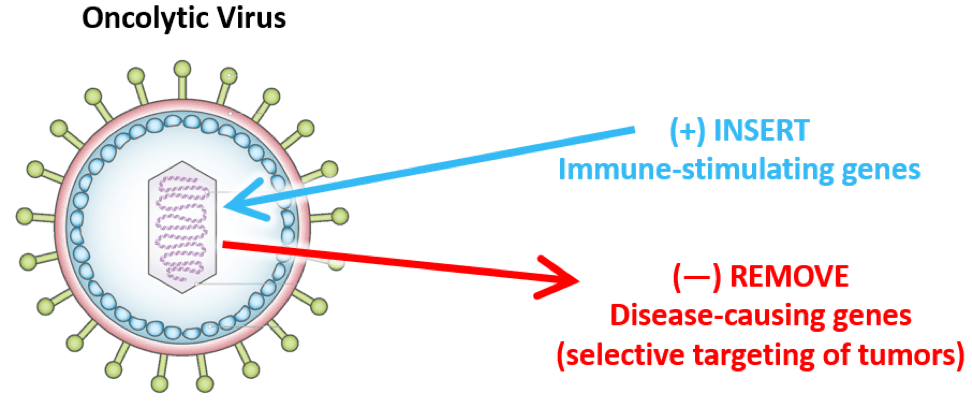
病毒竟能杀死癌细胞?溶瘤病毒“以毒攻癌”,肝癌患者生存期显著延长!
癌症治疗领域正经历前所未有的变革,从传统的手术、放疗、化疗,到免疫检查点抑制剂、CAR-T细胞疗法等,癌症治疗技术不断涌现。其中,溶瘤病毒疗法作为一种创新抗癌手段,近年来引起了人们的极大关注。
免疫管家 2025-06-18

国际前沿质子疗法免费临床!质子治疗创造“肿瘤缩小甚至消失”的奇迹,3年总生存率高达95%!
质子疗法,是一种使用质子束将辐射直接传递到肿瘤的放射治疗。质子疗法的优点是医生可以控制质子在哪里释放其抗癌能量。当质子穿过身体时,它们减速并与电子相互作用,释放能量。能量释放最高的点是“布拉格峰”,医生可以指定布拉格峰的位置,对目标肿瘤细胞造成最大的损害。质子束符合肿瘤的形状和深度,同时不伤害健康的组织和器官。
免疫管家 2025-06-11

FDA批准首款TIL疗法后,国产TIL细胞产品LM103在2025 ASCO公布惊艳数据,这些癌症患者或可获益!
近年来,新的治疗技术和方法不断涌现,为无数患者带来了生的希望。其中,肿瘤浸润淋巴细胞(TIL)疗法作为一种新兴的免疫治疗手段,正逐渐崭露头角,成为癌症治疗领域的研究热点。
免疫管家 2025-06-06

中生复诺健溶瘤病毒产品VG161亮相2025 ASCO
2025年美国临床肿瘤学会(ASCO)年会在芝加哥隆重召开,作为全球最具影响力的肿瘤学盛会,每年都会吸引来自世界各地的顶尖肿瘤专家、学者、科研人员以及药企代表齐聚一堂。在这里,他们分享最新的研究成果、探讨最前沿的治疗理念,共同推动肿瘤治疗技术的不断进步。
免疫管家 2025-06-05

肿瘤缩小69.2%!溶瘤病毒爆发,在卵巢癌、黑色素瘤、血液肿瘤中显示显著疗效
在漫长的癌症治疗过程中,手术、放疗和化疗等传统方法发挥了至关重要的作用,但它们仍然面临着巨大的局限性——特别是对于晚期、复发或难治性癌症患者。近年来,溶瘤病毒(OVs)作为一种新型的抗癌疗法,受到越来越多的关注。溶瘤病毒(OVs),包括腺病毒、新城疫病毒(NDV)、细小病毒和呼肠孤病毒,是天然存在的或遗传修饰的病毒,能...
免疫管家 2025-05-28

晚期鼻窦黏膜黑色素瘤经TILT-123联合TIL免疫治疗实现病理学完全缓解
2024年8月12日,《Immuno-Oncology and Technology》介绍了一例 48 岁的转移性鼻窦粘膜黑色素瘤女性患者,接受单次输注 TIL和多次注射溶瘤病毒 TILT-123(igrelimogene litadenorepvec)后实现持久的完全病理反应。
免疫管家 2025-05-21

20个月无瘤生存!溶瘤病毒疗法临床试验数据亮眼,多款产品效果显著
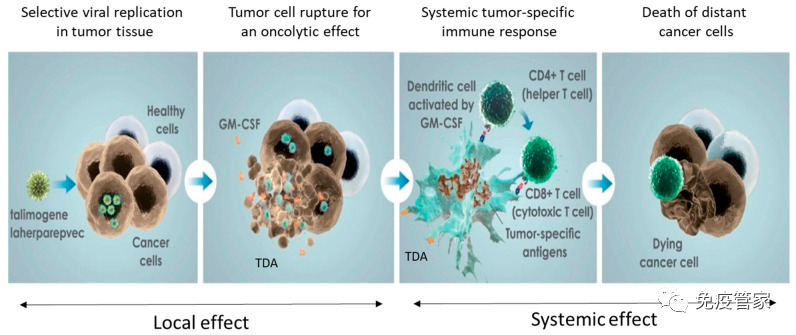
溶瘤病毒是一类能够选择性感染并杀死癌细胞的病毒,这些微小的病毒渗透到癌细胞中,复制并最终导致细胞破裂,同时激活身体的免疫系统加入战斗,最终达成抗癌效果。
免疫管家 2025-04-27

评价注射用重组人PD-1抗体单纯疱疹病毒(rHSV-1-APD1)治疗晚期肝细胞癌的安全性、生物分布和初步疗效的单臂、剂量爬坡Ⅰ期临床研究
评价注射用重组人PD-1抗体单纯疱疹病毒(rHSV-1-APD1)治疗晚期肝细胞癌的安全性、生物分布和初步疗效的单臂、剂量爬坡Ⅰ期临床研究
免疫管家 2025-04-21