相关推荐

PD-L1/VEGFR2双抗ADC药物JSKN027 Ⅰ期临床研究完成首例患者给药
3月17日,康宁杰瑞宣布其自主研发的PD-L1/VEGFR2双特异性抗体偶联药物(ADC)JSKN027治疗晚期恶性实体瘤的Ⅰ期临床研究(研究编号:JSKN027-101)已完成首例患者给药。
免疫管家 2026-03-17

面对癌症复发,我们还有多少底牌?这款ADC药物为小细胞肺癌患者带来超63%的缓解率!
3月10日,国家药品监督管理局药品审评中心(CDE)显示:注射用YL201拟纳入突破性治疗,拟定适应症为联合斯鲁利单抗用于广泛期小细胞肺癌的一线治疗。
免疫管家 2026-03-16

注射用YL201拟纳入突破性治疗
3月10日,国家药品监督管理局药品审评中心(CDE)显示:注射用YL201拟纳入突破性治疗,拟定适应症为联合斯鲁利单抗用于广泛期小细胞肺癌的一线治疗。
免疫管家 2026-03-12

德曲妥珠单抗用于HER2表达为IHC 3+的成人实体瘤患者适应症拟纳入优先审评
3月10日,国家药品监督管理局药品审评中心(CDE)显示:注射用德曲妥珠单抗(T-DXd, DS-8201a)拟纳入优先审评,用于治疗既往接受过治疗或无满意替代治疗方案的不可切除或转移性HER2表达为IHC 3+的成人实体瘤患者。
免疫管家 2026-03-12

注射用德曲妥珠单抗(T-DXd, DS-8201a)拟纳入优先审评
3月10日,国家药品监督管理局药品审评中心(CDE)显示:注射用德曲妥珠单抗(T-DXd, DS-8201a)拟纳入优先审评,用于接受抗HER2新辅助治疗后仍残存侵袭性病灶的HER2阳性成人乳腺癌患者的治疗。
免疫管家 2026-03-11

美国FDA授予AMT-253孤儿药资格认定
近日,美国食品药品监督管理局(FDA)授予普众发现关键产品AMT-253(靶向MUC18抗体偶联药物ADC)孤儿药资格认定,用于治疗软组织肉瘤。
免疫管家 2026-03-11

国产“生物导弹”突围!新一代ADC药物正在创造“奇迹”,晚期卵巢癌不是终点!
近日,在第27届欧洲妇科肿瘤学大会(ESGO 2026)上,翰森制药公布其靶向B7-H4的ADC药物Mocertatug rezetecan(HS-20089)的最新数据。 结果显示:在一项II期研究中,HS-20089单药治疗重度经治的铂敏感复发患者确认的客观缓解率(cORR)高达64.5%,意味着超过六成患者...
免疫管家 2026-03-09

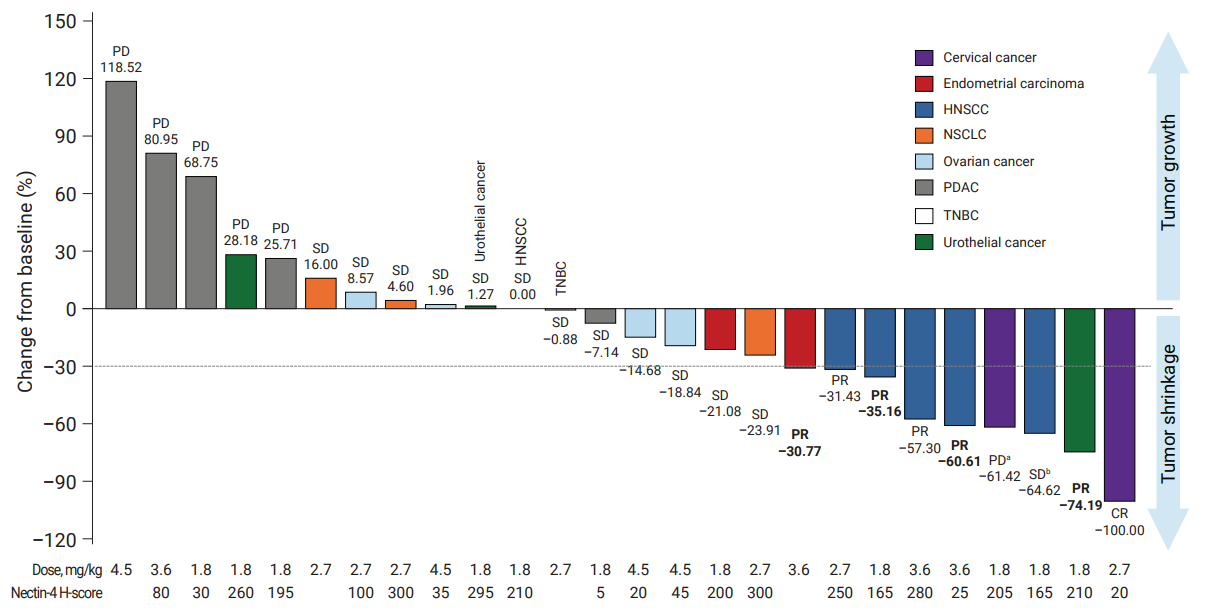
Risvutatug rezetecan在经治晚期实体瘤患者中的首次人体 Ia/b期研究结果公布
近日,《Cancer Cell》发表了Risvutatug rezetecan(研发代码HS-20093 / GSK5764227)在经治晚期实体瘤患者中的首次人体 Ia/b期研究(ARTEMIS-001研究,NCT05276609)结果。
免疫管家 2026-03-06

维迪西妥单抗联合免疫新辅助治疗膀胱癌研究数据亮相2026 ASCO-GU
近日,在美国旧金山举行的2026年美国临床肿瘤学会泌尿生殖系统肿瘤研讨会(ASCO-GU)上,荣昌生物公布了维迪西妥单抗联合特瑞普利单抗用于新辅助治疗HER2表达肌层浸润性膀胱癌(MIBC)Ⅱ期临床研究(RC48-C017)。结果显示,该联合疗法新辅助阶段表现出持久的疾病控制与生存获益,且安全性良好,为未来临床实践提供...
免疫管家 2026-03-03

Mocertatug Rezetecan(B7-H4 ADC)临床研究数据亮相ESGO 2026
近日,翰森制药宣布其在第27届欧洲妇科肿瘤学大会(ESGO 2026)上发布了两项评估mocertatug rezetecan(HS-20089 / GSK5733584)的临床研究数据。
免疫管家 2026-03-02