相关推荐

YL201用于晚期实体瘤的 1/1b 期试验数据登《自然医学》
3月13日,《自然医学》发表了靶向 B7H3 的抗体-药物偶联物YL201用于晚期实体瘤的 1/1b 期试验数据。
免疫管家 2025-03-20

注射用SHR-A1811拟纳入突破性治疗
3月19日,国家药品监督管理局药品审评中心(CDE)显示:恒瑞医药申请的注射用SHR-A1811拟纳入突破性治疗,用于既往接受含铂化疗及免疫检查点抑制剂治疗失败的HER2表达(IHC≥1+)的复发或转移性宫颈癌。这是瑞康曲妥珠单抗第8次纳入拟突破性治疗品种。
免疫管家 2025-03-20

在研 Rinatabart Sesutecan (Rina-S®) 在晚期卵巢癌患者中继续显示出令人鼓舞的抗肿瘤活性
3月17日,Genmab A/S公布了 rinatabart sesutecan (Rina-S) 的 1/2 期 RAINFOL-01 研究队列 B1 的最新数据。rinatabart sesutecan (Rina-S) 是一种研究性叶酸受体-α (FRα) 靶向的 TOPO1 抗体-药物偶联物 (ADC),RAI...
免疫管家 2025-03-19
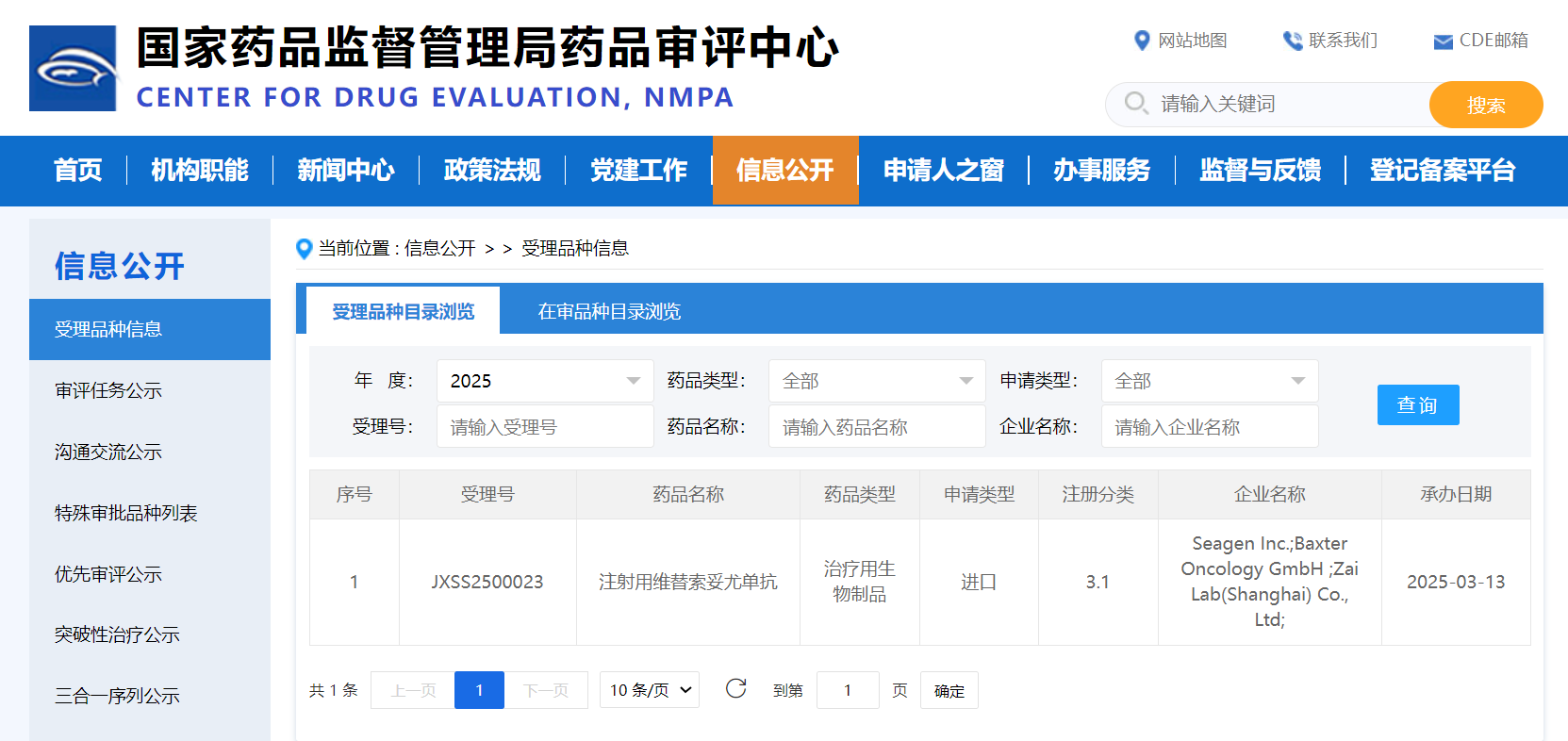
再鼎医药的维替索妥尤单抗的生物制品许可申请获受理
3月13日,国家药品监督管理局药品审评中心显示:再鼎医药的维替索妥尤单抗用于治疗系统性治疗期间或之后病情进展的复发或转移性宫颈癌患者的生物制品许可申请获受理。
免疫管家 2025-03-13

注射用JSKN003拟纳入突破性治疗
3月10日,国家药品监督管理局药品审评中心(CDE)显示:注射用JSKN003拟纳入突破性治疗,用于治疗铂耐药复发性上皮性卵巢癌、原发性腹膜癌或输卵管癌。
免疫管家 2025-03-12
惊爆!爆款抗癌“神药”抗体偶联药物(ADC)掀起抗癌风暴,鼻咽癌、头颈癌、卵巢癌、乳腺癌患者有救啦!
3月7日,注射用维贝柯妥塔单抗(MRG003)拟纳入优先审评,适用于既往经至少二线系统化疗和PD-1/PD-L1抑制剂治疗失败的复发/转移性鼻咽癌患者。
免疫管家 2025-03-12

注射用维贝柯妥塔单抗拟纳入优先审评
3月7日,国家药品监督管理局药品审评中心(CDE)显示:乐普生物申请的注射用维贝柯妥塔单抗拟纳入优先审评,适用于既往经至少二线系统化疗和PD-1/PD-L1抑制剂治疗失败的复发/转移性鼻咽癌患者。
免疫管家 2025-03-11
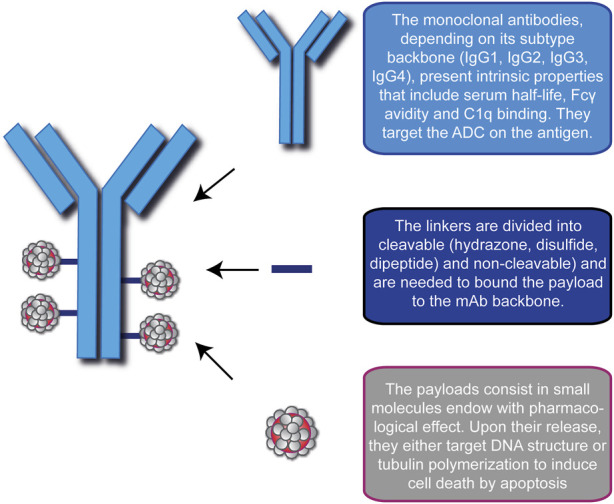
抗体偶联药物强势来袭,实体瘤治疗大突破,ADC药物成头颈癌、肺癌、尿路上皮癌、胰腺癌“香饽饽”
近日,美国食品和药物管理局(FDA)授予PYX-201快速通道资格,用于治疗接受铂类化疗以及和抗PD-1/PD-L1疗法后疾病进展复发性或转移性头颈部鳞状细胞癌 (R/M HNSCC) 成年患者。
免疫管家 2025-03-06
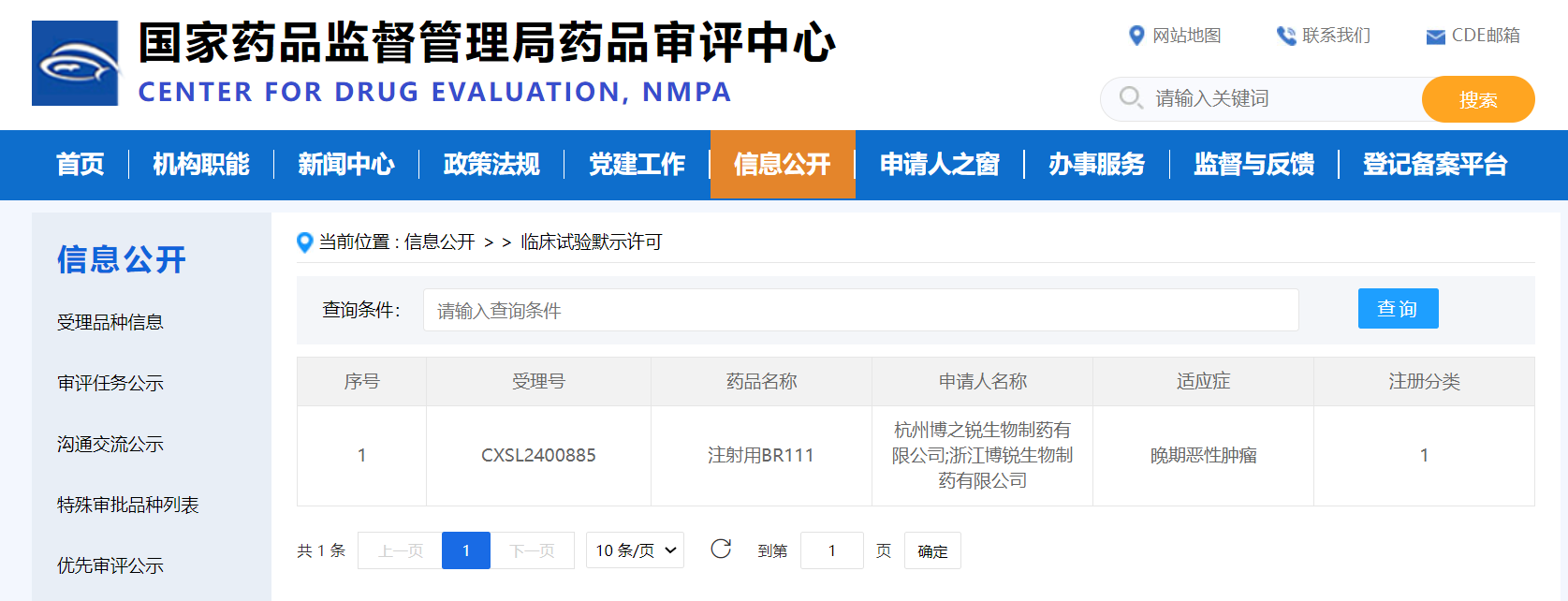
ADC药物注射用BR111获批临床
3月4日,浙江博锐生物宣布其自主研发的1类创新型治疗用生物制品注射用BR111正式获得国家药品监督管理局(NMPA)的临床试验批准,晚期恶性肿瘤。BR111是全球第一个获批临床的抗ROR1双表位ADC。
免疫管家 2025-03-05

美国FDA授予PYX-201 快速通道资格
2 月 26 日,Pyxis Oncology宣布,美国食品和药物管理局 (FDA) 已授予 PYX-201 快速通道资格,用于治疗复发性或转移性头颈部鳞状细胞癌 (R/M HNSCC) 成年患者,这些患者在接受铂类化疗后疾病进展,并且抗 PD-(L)1 抗体。
免疫管家 2025-03-03