相关推荐
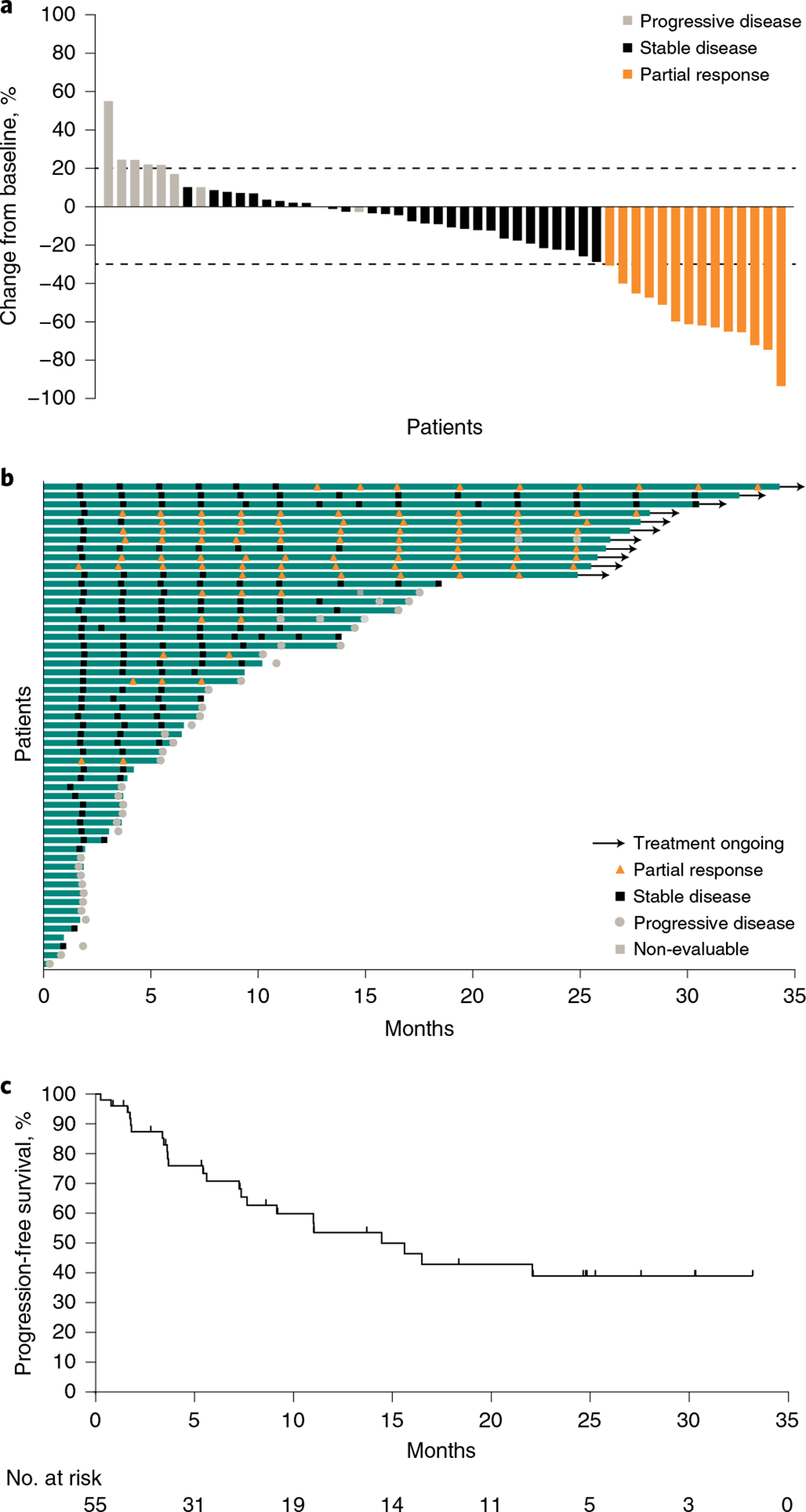
治疗32个月无进展!CAR-NK细胞疗法升级抗癌力,精准杀癌,已有患者肿瘤缩小超50%
几十年来,手术,放疗和化疗一直是癌症治疗的主要手段。然而,近年来,免疫检查点抑制剂和细胞疗法逐渐成为有前途的治疗方法。这些创新疗法巧妙地利用我们的免疫系统来消除癌细胞。
免疫管家 2025-09-12

美国FDA批准belzutifan用于嗜铬细胞瘤或副神经节瘤
5月14日,美国食品药品监督管理局(FDA)批准belzutifan用于成人和12岁及以上的局部晚期、不可切除或转移性嗜铬细胞瘤或副神经节瘤(PPGL)患者。这是 FDA 首次批准口服 PPGL 疗法。
免疫管家 2025-05-15

IBR854细胞注射液联合培唑帕尼用于晚期肾细胞癌的II期临床研究获得NMPA临床默示许可
2025年4月18日,英百瑞宣布其IBR854细胞注射液(靶点:5T4)联合培唑帕尼用于治疗晚期肾细胞癌的 II期临床研究获得国家药品监督管理局(NMPA)临床默示许可。
免疫管家 2025-04-21

casdatifan治疗透明细胞肾细胞癌1/1b 期研究显示出良好反应
2025 年美国临床肿瘤学会 (ASCO) 泌尿生殖系统 (GU) 癌症研讨会上公布了ARC-20 研究(NCT05536141)的数据。ARC-20 是 HIF-2a 抑制剂casdatifan治疗透明细胞肾细胞癌 (ccRCC) 的 1/1b 期研究。
免疫管家 2025-02-21
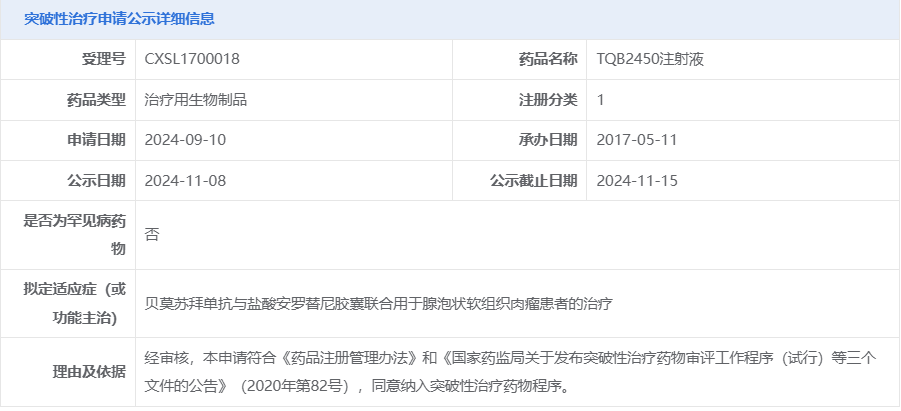
贝莫苏拜单抗和安罗替尼联合疗法拟纳入突破性治疗品种
11月8日,国家药品监督管理局药品审品中心(CDE)显示:贝莫苏拜单抗(TQB2450)拟纳入突破性治疗品种,拟定适应症为联合盐酸安罗替尼胶囊用于腺泡状软组织肉瘤患者的治疗。
免疫管家 2024-11-13

中位生存期为21.4个月!Belzutifan亮相《新英格兰医学杂志》,肾癌患者新的治疗选择
8月21日,《新英格兰医学杂志》发表了一篇题为“Belzutifan versus Everolimus for Advanced Renal-Cell Carcinoma”的研究论文,文中介绍了Belzutifan(贝组替凡)治疗肾细胞癌的III期LITESPARK-005试验结果。
免疫管家 2024-08-27

Belzutifan(贝组替凡,Welireg)治疗肾细胞癌的III期LITESPARK-005试验结果登《新英格兰医学杂志》
8月21日,《新英格兰医学杂志》发表了一篇题为“Belzutifan versus Everolimus for Advanced Renal-Cell Carcinoma”的研究论文,文中介绍了Belzutifan(贝组替凡,Welireg,)治疗肾细胞癌的III期LITESPARK-005试验结果。
免疫管家 2024-08-23

抗CD70-CAR-T(anti-CD70-CAR-T)细胞注射液治疗CD70+不可手术切除的局部晚期或复发/转移性肾细胞癌患者的安全性和有效性的探索性临床研究
抗CD70-CAR-T(anti-CD70-CAR-T)细胞注射液治疗CD70+不可手术切除的局部晚期或复发/转移性肾细胞癌患者的安全性和有效性的探索性临床研究
免疫管家 2024-08-07