相关推荐

BTK抑制剂洛布替尼研究新成果亮相2025 ASH
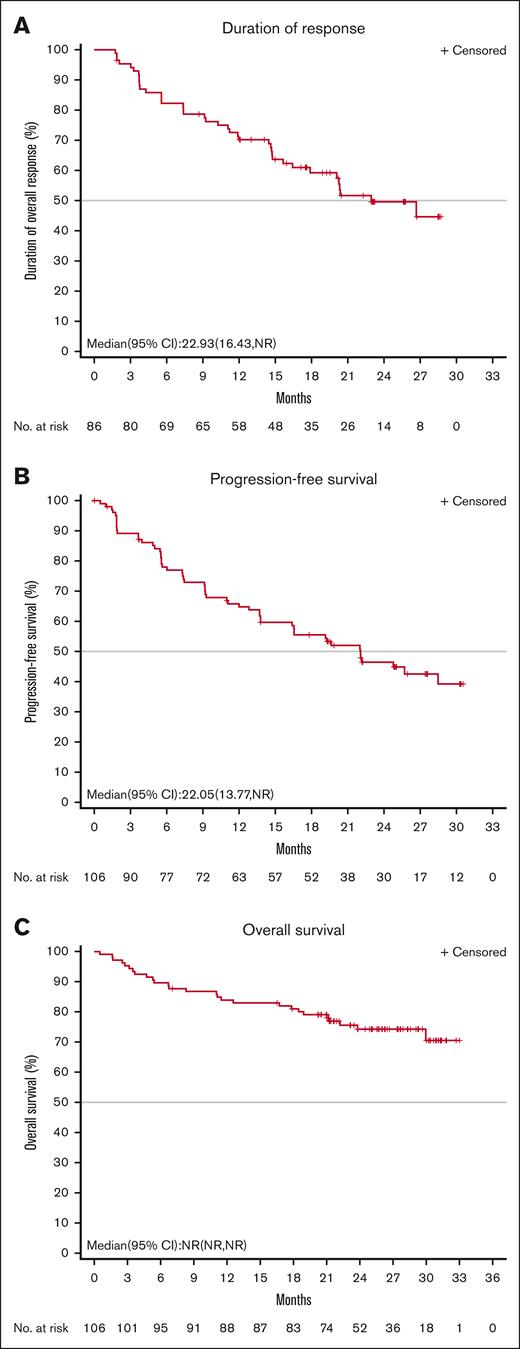
ASH(美国血液学会)年会是全球血液学领域规模最大的国际学术盛会之一,汇集了最前沿的研究进展及最新的药物研发数据,展示全球血液学领域的最高学术水平。第67届ASH年会上,麓鹏制药公布了全球首个且唯一的第四代共价兼非共价BTK抑制剂洛布替尼(LP-168)治疗既往接受过BTK抑制剂治疗的复发或难治性套细胞淋巴瘤患者的RO...
免疫管家 2025-12-10

新型BTK抑制剂奥布替尼和坦昔妥单抗的多项研究数据亮相2025 ESMO
近日,2025年欧洲肿瘤内科学会(ESMO)年会在德国柏林召开。此次会议上,诺诚健华公布了新型BTK抑制剂奥布替尼和坦昔妥单抗的多项研究数据。
免疫管家 2025-10-17

洛布替尼纳入优先审评
近日,国家药监局药品审评中心(CDE)显示:麓鹏制药申报的洛布替尼片(Rocbrutinib)已纳入优先审评,适用于既往接受过布鲁顿氏酪氨酸激酶(BTK)抑制剂治疗的成人套细胞淋巴瘤(MCL)患者。
免疫管家 2025-05-19