9月25日,华昊中天宣布,其核心产品优替德隆再次被美国食品药品监督管理局(FDA)授予孤儿药资格认定,适应症为胰腺癌。这是继乳腺癌脑转移和胃癌之后,优替德隆被FDA授予的第三项孤儿药资格。
胰腺癌是一种恶性度较高的肿瘤,因其早期症状隐匿、诊断困难、进展快、侵袭性强、预后不良等特点,被誉为“癌中之王”。五年生存率仅为10%左右,远低于其他常见癌症,是所有恶性肿瘤中最低的。
2024年CSCO年会上,百泰生物公布了其一项多中心、单臂II期临床研究的初步结果,该研究旨在评估Utidelone联合吉西他滨作为不可切除的晚期胰腺癌一线治疗的疗效。截至报告日期,共入组了20例不可切除且不适合局部治疗的晚期胰腺癌患者,其中11例已完成首次疗效评估。在这些患者中,3例达到部分缓解(PR),5例达到疾病稳定(SD);客观缓解率(ORR)为27.27%,疾病控制率(DCR)达到72.72%。中位总生存期(mOS)为9.57个月。
优替德隆(utidelone)是埃博霉素类衍生物和新一代微管抑制剂,此前已在中国获批治疗既往接受过至少一种化疗方案的复发或转移性乳腺癌。
2025美国临床肿瘤学会(ASCO)年会上公布了新型口服微管抑制剂优替德隆胶囊(UTD2)单药治疗晚期实体瘤患者的美国多中心Ⅰ期研究数据(Abstract 3030)。共有11例患者完成疗效评估,其中疾病完全缓解(CR)1例(卵巢癌)、疾病部分缓解(PR)1例(卵巢癌)、疾病稳定(SD)7例(非小细胞肺癌2例;胰腺癌2例;睾丸癌、阑尾腺癌及软组织肉瘤各1例),客观缓解率(ORR)为18.2%,临床获益率(CBR)达81.8%。
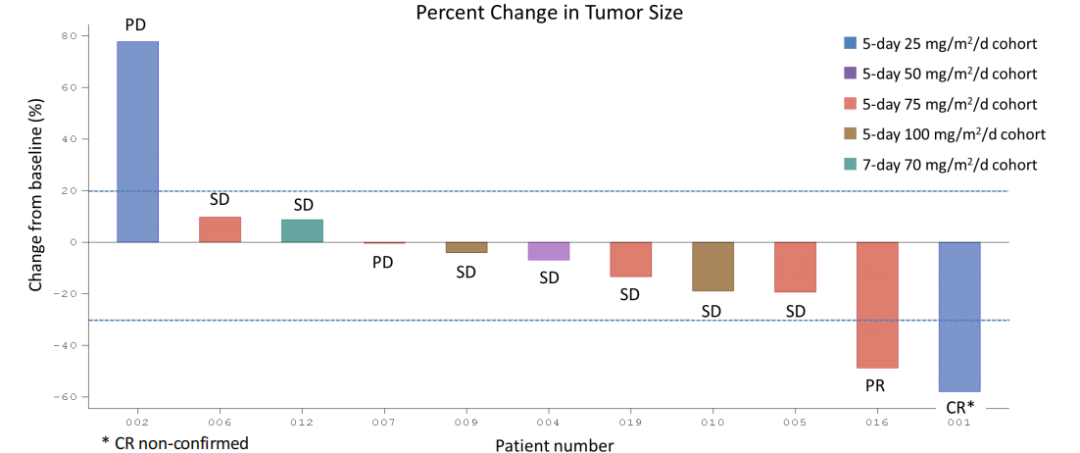
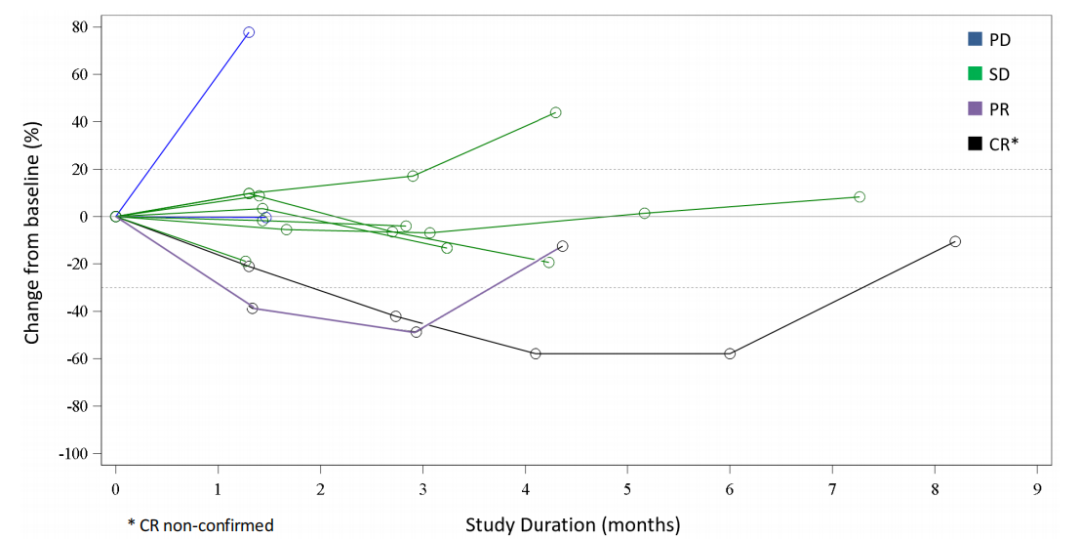
一名54岁白人女性,2011年4月确诊Ⅲ期卵巢癌。2011年4月5日行双侧输卵管卵巢切除术、大网膜切除术及经腹子宫切除术。2011年5月至2023年4月期间接受过7线晚期治疗,包括化疗、贝伐珠单抗、奥拉帕利及帕博利珠单抗。入组本研究时肿瘤已转移至腹腔淋巴结。2023年6月12日起首次接受UTD2单药治疗(25 mg/m²/天-5天给药),共接受12个周期给药,末次治疗时间为2024年2月2日。疗效评估显示:第3周期第1天(C3D1)SD,第5周期第1天(C5D1)部分缓解PR,第7周期第1天(C7D1)部分缓解PR,第9周期第1天(C9D1)完全缓解CR,治疗结束时疾病进展(PD)。

临床试验对于传统疗法无效或疗效较差的患者来说,是寻找新的治疗药物和方法的,最快最安全的途径,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。目前有临床试验正在寻找患者,患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家(400-880-3716)来寻找适合的临床研究。

相关推荐
随便看看
- 泰瑞沙(通用名:甲磺酸奥希替尼片以下简称“奥希替尼”)术后辅助治疗适应症成功准入医保目录
- PC-002获得快速通道资格,用于治疗伯基特淋巴瘤
- JBI-778 在实体瘤中的 I 期临床试验中实现首批患者给药
- 依沃西单抗III期HARMONi-6研究显示阳性结果
- 总生存率高达99%!纳武利尤单抗联合AVD化疗方案延长霍奇金淋巴瘤患者无进展生存期
- Dato-DXd在国内获批上市
- KRAS G12C抑制剂D3S-001最新临床研究成果荣登国际顶级期刊《Nature Medicine》
- KRAS基因靶点药物不间断研究中
- 惊喜!无侵袭性癌生存率达到88.3%,一文读懂15款抗体偶联ADC药物
- 欧狄沃再添可切除肺癌新适应症











