作者:小编
更新时间:2025-12-04
点击数:
12月3日,美国食品药品监督管理局(FDA)批准吡托布鲁替尼(Pirtobrutinib)用于曾接受过共价BTK抑制剂治疗的复发或难治性慢性淋巴细胞白血病或小淋巴细胞淋巴瘤(CLL/SLL)成人患者。

在吡托布鲁替尼(Pirtobrutinib)联合Idelalisib/利妥昔单抗或苯达莫司汀/利妥昔单抗治疗经共价布鲁顿酪氨酸激酶抑制剂预处理后的慢性淋巴细胞白血病/小淋巴细胞淋巴瘤的3期试验中,238例复发或难治性慢性淋巴细胞白血病/小淋巴细胞淋巴瘤(R/R CLL/SLL)患者被随机分配接受吡托布鲁替尼治疗(n = 119)或研究者选择方案治疗(n = 119),后者包括伊德拉利塞联合利妥昔单抗(IdelaR,n = 82)或苯达莫司汀联合利妥昔单抗(BR,n = 37),以下简称IdelaR/BR方案。
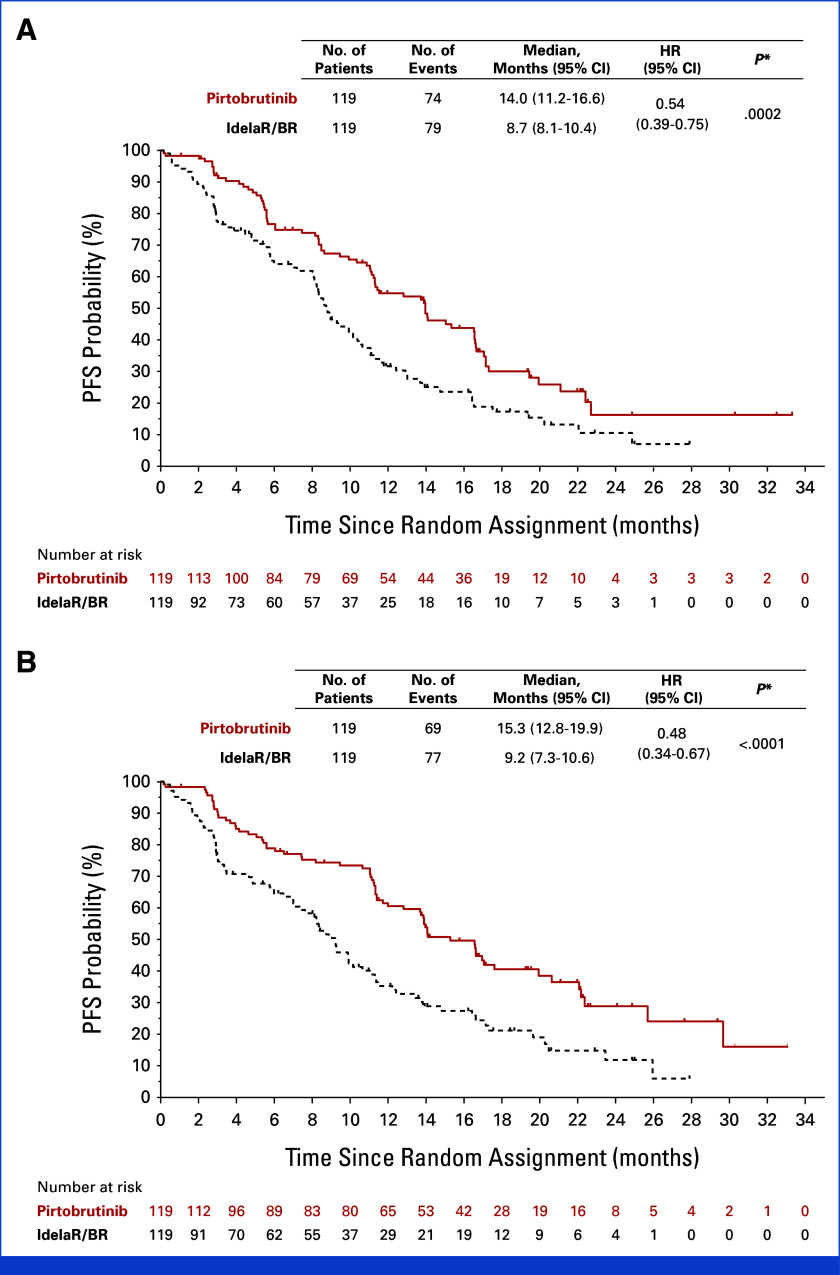
结果显示:吡托布鲁替尼疗效优于IdelaR/BR方案。在中位随访时间达17.2个月的最终总生存期分析中,吡托布鲁替尼组的中位IRC-PFS为14个月,而IdelaR/BR组为8.7个月,表明吡托布鲁替尼将疾病复发、进展或死亡风险相对降低了46%。
研究者评估的无进展生存期(INV-PFS)与IRC评估结果高度一致:吡托布鲁替尼组中位PFS为15.3个月,IdelaR/BR组为9.2个月。
临床试验对于传统疗法无效或疗效较差的患者来说,是寻找新的治疗药物和方法的,最快最安全的途径,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。目前有临床试验正在寻找患者,患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。对临床试验有兴趣或需要帮助的患者可提交病历资料至康和源免疫之家(400-880-3716)来寻找适合的临床研究。












