2月4日,《nature medicine》发表了瑞普替尼(Repotrectinib)用于NTRK融合阳性晚期实体肿瘤患者的1/2期TRIDENT-1临床试验结果。

这项临床试验共招募144名NTRK实体瘤患者。在未接受过TKI治疗的患者队列(51例)中,中位随访时间为25.7个月。确认的客观缓解率为59%(30例),其中完全缓解8例(16%),部分缓解22例(43%)。中位至缓解时间为1.8个月。缓解不受肿瘤类型、NTRK基因或融合伴侣影响。中位缓解持续时间未达到,85%的缓解者缓解持续至少24个月。中位无进展生存期为30.3个月,60%的患者在24个月时无疾病进展。24个月总生存率为68%,总生存数据尚不成熟。在18例未接受过全身治疗的患者中,缓解率为61%;在27例NTRK融合非小细胞肺癌患者中,缓解率为63%。
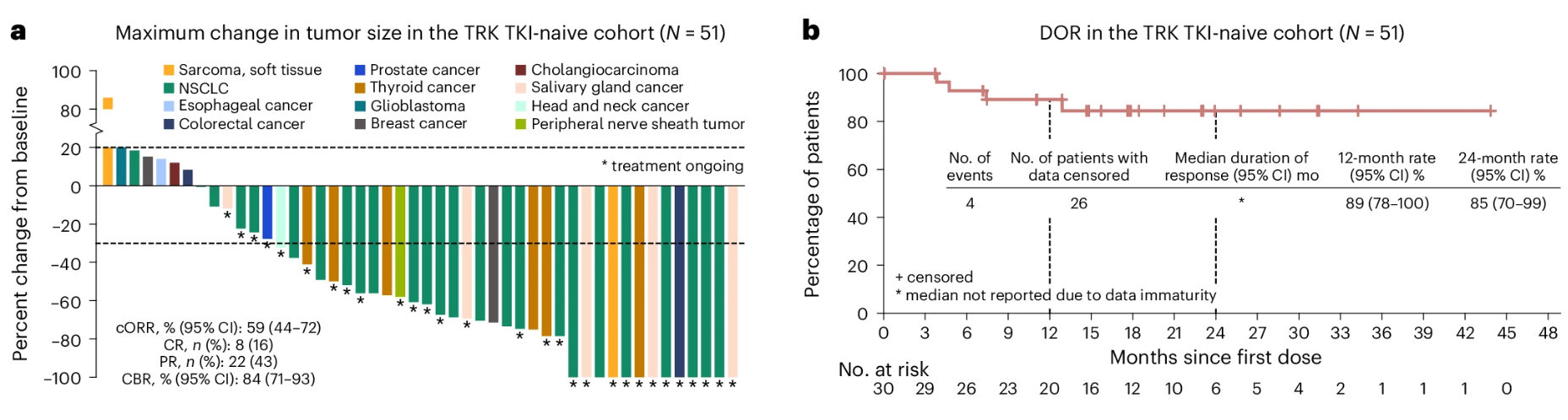
在接受过TKI治疗的患者队列(69例)中,63例(91%)末次治疗为TKI,其中56例(89%)因疾病进展停药。中位随访时间为21.3个月。确认的客观缓解率为48%(33例),其中完全缓解2例(3%),部分缓解31例(45%)。中位至缓解时间为1.9个月,中位缓解持续时间为9.8个月,42%的缓解者缓解持续至少12个月。缓解同样不受肿瘤类型、NTRK基因或融合伴侣影响。中位无进展生存期为7.4个月,26%的患者在12个月时无疾病进展。中位总生存期为18.6个月,12个月总生存率为62%。既往TKI治疗史:46%曾接受恩曲替尼,52%曾接受拉罗替尼;在既往接受恩曲替尼的32例患者中,确认缓解率为56%(18例);在既往接受拉罗替尼的36例患者中,确认缓解率为39%(14例)。在17例NTRK融合非小细胞肺癌患者中,缓解率为53%。

幸运的是,NTRK抑制剂佐来曲替尼相关的临床试验正在招募患者。参与经国家药监局批准的正式临床试验,意味着患者有机会免费接受这种前沿靶向药物治疗,由顶尖医院的专家团队进行全程管理和监测。这不仅能大大减轻家庭的经济负担,更是获得最新治疗机会的重要途径。对正在开展的佐来曲替尼等NTRK靶向药临床试验感兴趣,希望评估入组的患者请联系康和源免疫之家(400-880-3716)。

相关推荐
随便看看
- 依沃西单抗联合化疗方案一线治疗晚期鳞状非小细胞肺癌重磅研究结果公布
- 全球首创EGFR×HER3双抗ADC药物(BL-B01D1)用于食管鳞癌的Ib期研究登《自然医学》
- 依沃西单抗第二项肺癌适应症获批
- 美国FDA授予EO-3021 快速通道资格,用于 Claudin (CLDN)18.2的胃癌/胃食管结合部癌症
- PD-L1单抗度伐利尤涵盖肺癌、肝癌、尿路上皮癌、胆道癌、子宫内膜癌等多个适应症!
- Anixa Biosciences将在第 39 届SITC年会上展示乳腺癌疫苗 1 期研究的更多数据
- 生存超4年!ADC药物MRG002、DS-8201大放异彩,HER2实体瘤患者福音
- TQB2102拟纳入突破性治疗
- GPRC5D CAR-T产品RD118新药临床试验申请(IND)获批
- 舒沃替尼联合贝伐珠单抗的2期WU-KONG29临床数据亮相2025 WCLC











