相关推荐
汇总 | 一文看懂国内外已上市CAR-T细胞疗法产品,均惠及血液肿瘤患者
CAR-T细胞疗法是肿瘤免疫界的关注热点,通过基因改造工程来改变患者自身的T细胞,使其能够更高效率地识别、攻击癌细胞。
免疫管家 2024-10-28

国内首个!CAR-T细胞疗法瑞基奥仑赛获批用于治疗套细胞淋巴瘤,客观缓解率为81.36%
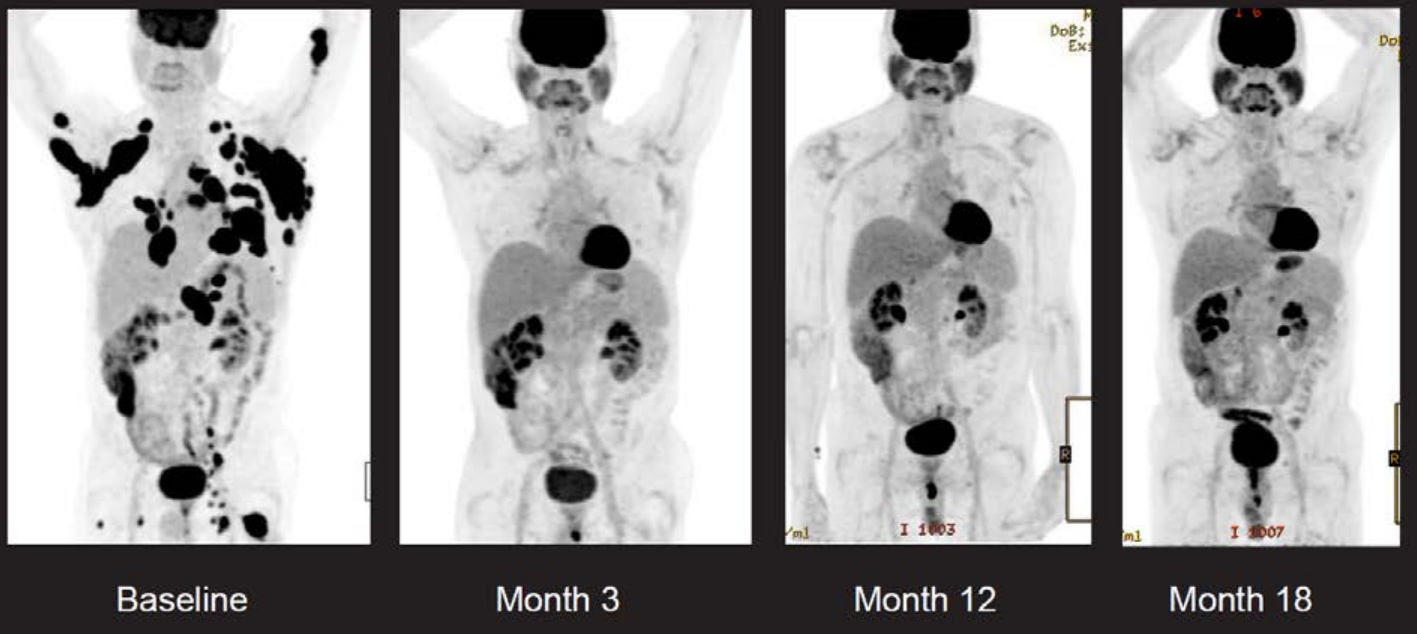
8月27日,国家药品监督管理局(NMPA)发布公告,批准CAR-T细胞治疗产品瑞基奥仑赛注射液新适应症上市申请,用于治疗经过包括布鲁顿酪氨酸激酶抑制剂(BTKi)治疗在内的二线及以上系统性治疗的成人复发或难治性套细胞淋巴瘤(r/r MCL)患者。这是首个在中国批准用于治疗r/r MCL患者的细胞治疗产品。
免疫管家 2024-08-28