5月10日,成都威斯津生物医药科技有限公司(WestGene)宣布,其mRNA治疗性癌症疫苗WGc-043获得FDA IND批准,这是一个历史性的里程碑。这一里程碑式的成就标志着全球首个EB病毒相关mRNA治疗性癌症疫苗获得批准。
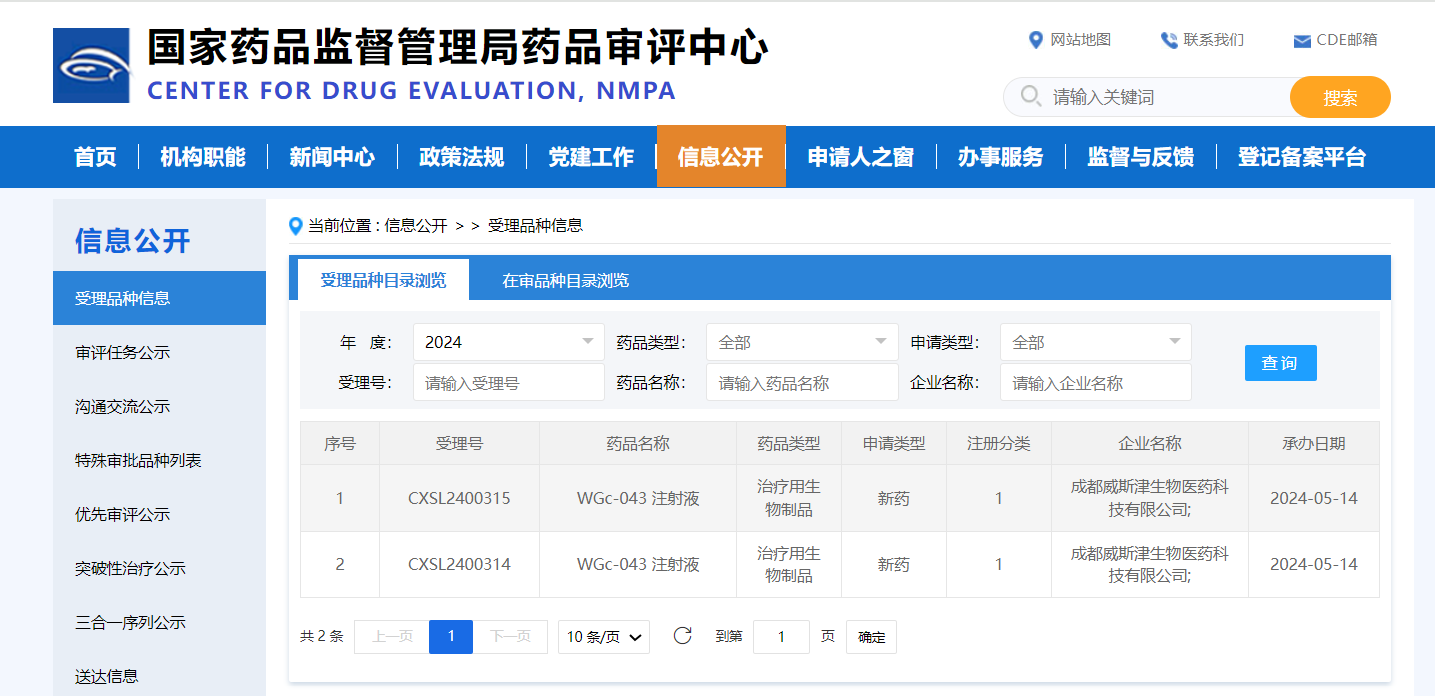
5月14日,国家药品监督管理局药品审评中心(CDE)官网公示,由成都威斯津生物医药科技有限公司(以下简称“威斯津生物”)研发的“WGc-043 注射液”新药临床试验(IND)申请获CDE受理,成为首个完成“中美双报”的EB病毒相关肿瘤mRNA治疗性疫苗。
当前mRNA领域最为核心的底层技术,包括递送载体、序列设计以及放大化生产等。目前,威斯津生物搭建了5大mRNA研发技术平台,布局60余项发明专利(国际专利21项),实现了完整自主知识产权。
WGc-043的抗原是优选的最为广谱、安全的蛋白序列;mRNA分子中引入了原创设计的免疫增强子(IE);mRNA递送载体为自主研发的已获得美国和欧洲专利授权的新型LNP(该LNP的安全性:已在3个品种的临床试验中得到验证)。使WGc-043能通过激活患者自身的抗肿瘤免疫,在体内生成杀伤肿瘤的细胞毒性T细胞(cytotoxic T cells,CTLs)、抗原特异性抗体以及记忆性T细胞,相当于CAR-T和单克隆抗体联合抗肿瘤的效果,还可避免肿瘤复发,具有更高效的抗癌效果及优越的安全性。
WGc-043自身的优势明显,高效低毒、通用性强,生产快速、价格便宜,拥有完整自主知识产权。在已完成的WGc-043针对鼻咽癌和自然杀伤T细胞淋巴瘤两个适应症的IIT(研究者发起的临床试验)中,展现出比现有公开的其它mRNA肿瘤治疗性疫苗更优越的安全性和有效性。一旦成功上市,WGc-043将为晚期EB病毒阳性实体瘤和血液恶性肿瘤患者提供新的治疗选择。

相关推荐
随便看看
- DM005新药临床研究申请获国家药监局批准
- 治疗仅4周,肿瘤明显缩小!舒沃替尼有效治疗EGFR 20号外显子插入突变非小细胞肺癌患者
- 里程碑!澳门首个获批治疗胆管癌的选择性FGFR受体酪氨酸激酶抑制剂--达伯坦®
- ADC药物ZL-1310获美国FDA 孤儿药资格认定
- 中国研究团队研究了信迪利单抗联合化疗对晚期食管鳞状细胞癌受试者的HRQoL方面的影响
- 疾病进展或死亡风险降低57%!inavolisib方案针对乳腺癌获突破性疗法认定
- ADC药物9MW2821、7MW3711、9MW2921的临床研究数据即将亮相2025年ASCO
- 正大天晴2款1类新药的临床试验申请获得受理
- QLC5508用于广泛期小细胞肺癌患者的I期临床试验结果亮相2025 WCLC
- 美国FDA批准度伐利尤单抗用于非小细胞肺癌











