热门推荐
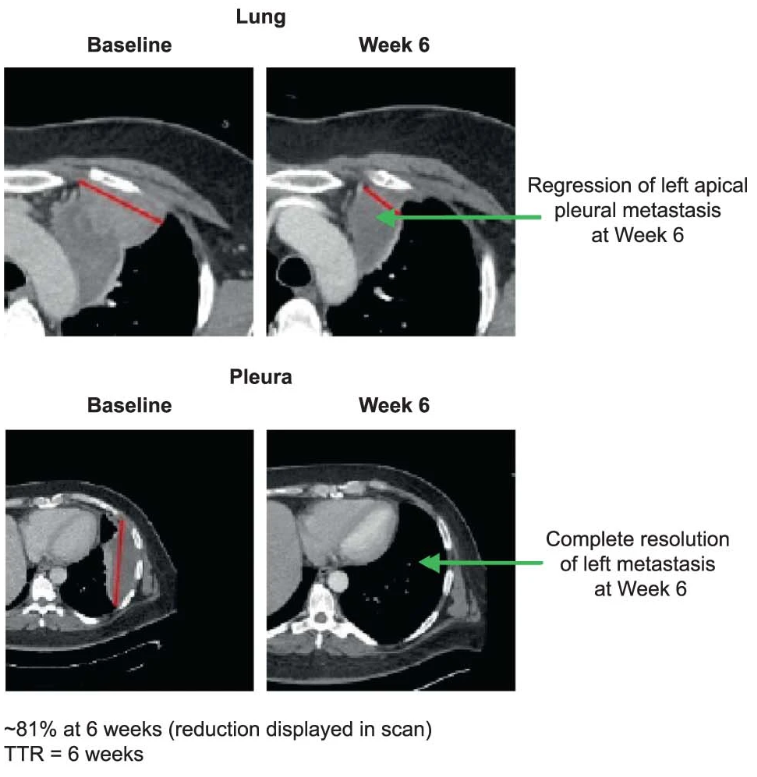
- 精 疾病控制率高达90%!TCR-T细胞横扫黑色素瘤、宫颈癌、肉瘤、肝癌等实体瘤,肿瘤缩小81%!
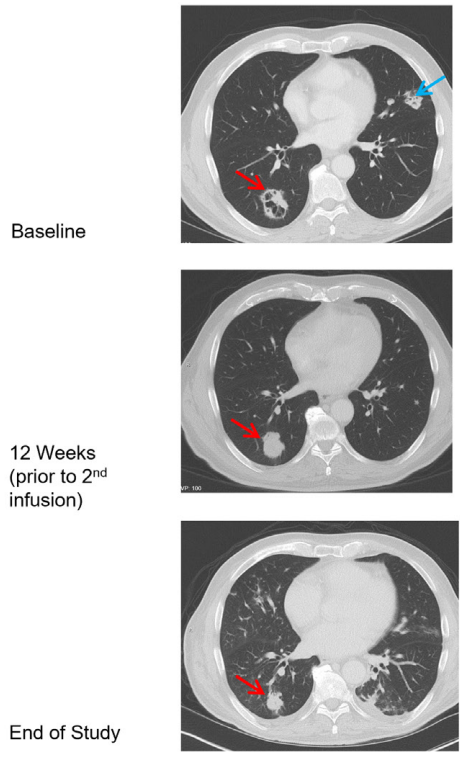
- 精 首款用于治疗实体瘤的TCR-T细胞疗法获批在即!非小细胞肺癌治疗43天肿瘤缩小
- 精 肿瘤新型杀伤武器-TCR-T细胞疗法在肝细胞癌、胰腺癌、卵巢癌、尿路上皮癌等癌种中前景广阔
- 精 87%患者肿瘤缩小!TCR-T疗法惠及滑膜肉瘤、黑色素瘤等实体瘤!
- 精 87% 患者肿瘤缩小!TCR-T疗法IMA203用以治疗经治转移性黑色素瘤患者的最新数据公布
- 精 治疗8个月约25个肺部肿瘤完全消退!TCR-T治疗在宫颈癌等多种HPV相关肿瘤中表现优异
- 精 TCR-T狙击手已到位,狙击宫颈癌,肝癌等多款实体瘤!
- 精 肝癌晚期怎么办?TCR-T和CAR-T细胞疗法迎来新希望
- 精 与CAR-T媲美的细胞疗法,看“显眼包”TCR-T如何攻击癌细胞?
- 精 攻克实体瘤哪家强,细胞疗法找TCRT
- 精 TCR-T细胞疗法针对实体瘤患者的临床试验开始了
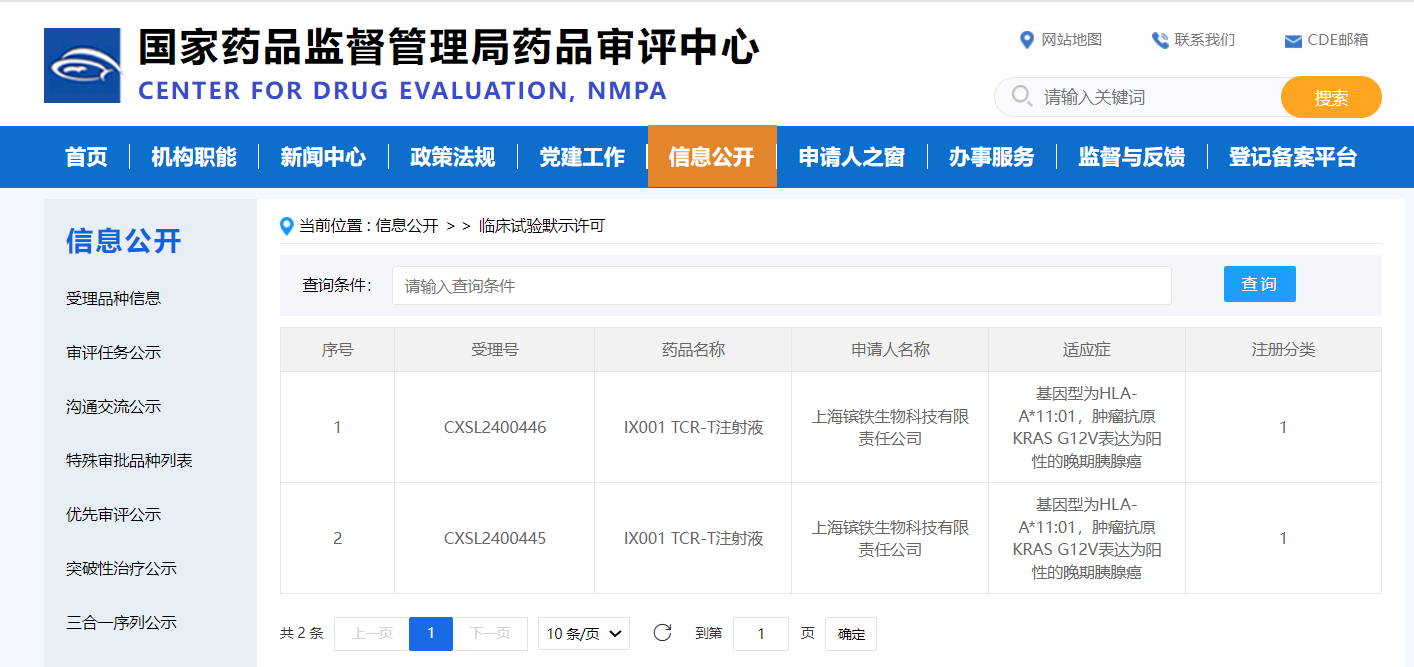
- 精 国内TCR-T细胞疗法获批临床
资讯列表
T细胞受体工程化T细胞疗法(TCR-T)是一种新型疗法,它通过使用患者自身的免疫细胞来对抗癌症。对于某些类型的癌症(如软组织肉瘤)患者来说,TCR-T细胞疗法是一种很有前途的疗法。
多年来,人类一直与狡猾的癌细胞进行战斗。随着时间的不断流逝,人类的抗癌技术也不断得到提升,手术-放化疗-靶向药物-免疫治疗等治疗手段层出不穷。近年来,一款T细胞受体工程化T细胞疗法(TCR-T)横空出世,成为了一款对抗癌症强有力的治疗手段。
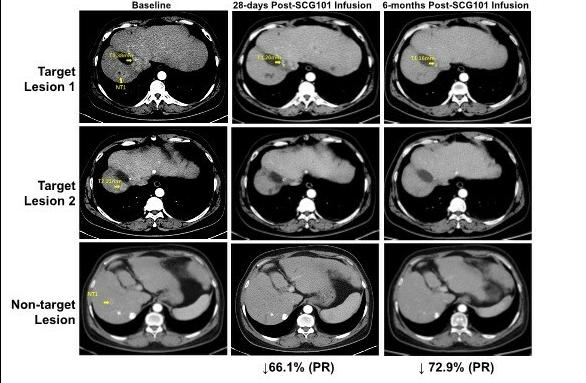
星汉德生物在EASL2025年会上公布的SCG101 TCR-T细胞疗法数据惊艳:这款针对乙肝表面抗原的自体T细胞疗法,通过基因编辑技术改造T细胞,实现抗病毒抗肿瘤双重效果。临床显示,94%患者病毒标志物显著下降,47%患者肿瘤缩小,中位生存期达10.6个月。北京协和医院案例证实,晚期患者单次输注后肿瘤缩小74.5%,...
2025年5月8日,荷兰阿姆斯特丹的欧洲肝病年会(EASL2025)上,星汉德生物的研究成果引爆全场—他们的SCG101 TCR-T细胞疗法在治疗晚期乙肝相关肝癌(HCC)的临床试验中,同时实现了抗病毒和抗肿瘤的双重奇迹。
随着CAR-T细胞疗法的“爆火”,NK、TIL、TCR-T等免疫细胞疗法也逐渐引得注意。其中TCR-T细胞疗法通过利用基因编辑技术改造患者外周血的T细胞,这种改造后的T细胞回输患者体内后能够发挥特异性识别和杀伤肿瘤细胞作用。在临床试验中已经展现出卓越的疗效,为实体肿瘤患者带来了希望。
2025年4月9日,《自然医学》(Nature Medicine)发表了IMA203 TCR-T疗法1期临床试验(NCT03686124)的中期分析结果。结果显示其在多种晚期实体瘤患者中表现出显著的抗肿瘤活性和可控的安全性。
近年来,癌症免疫治疗领域取得了突破性进展,其中T细胞受体工程化T细胞疗法(TCR-T)因其精准靶向肿瘤抗原的能力,成为继CAR-T疗法后的又一革命性技术。
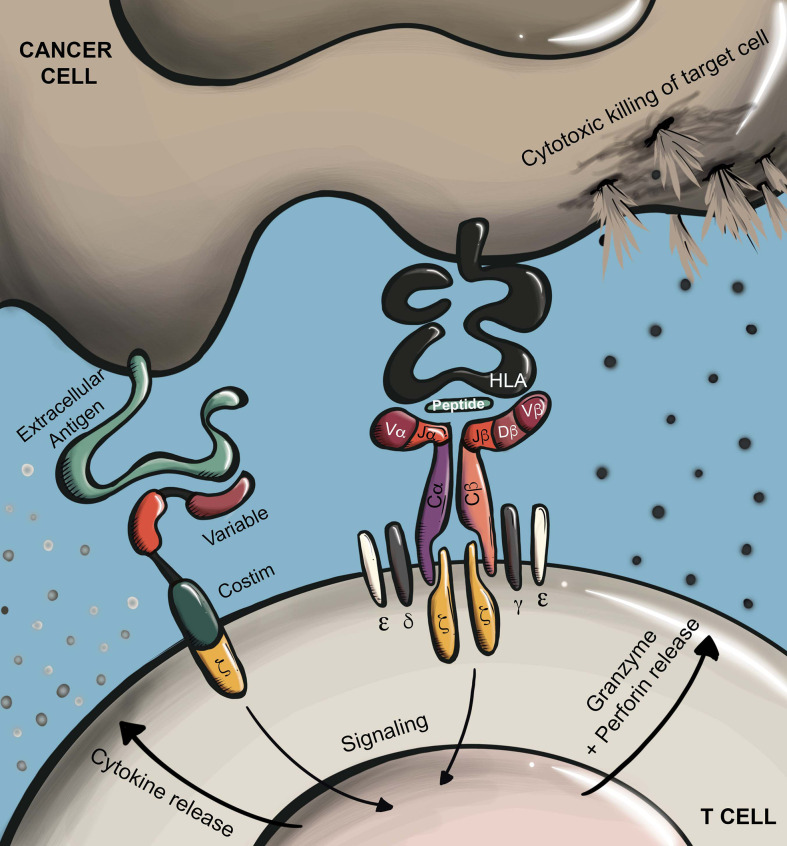
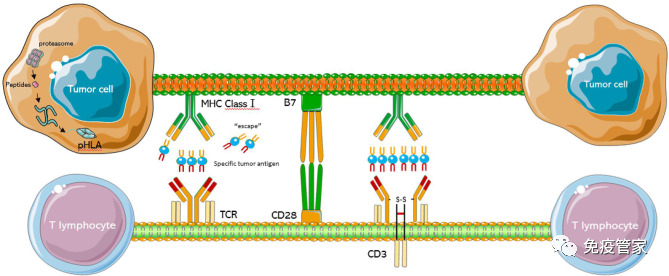
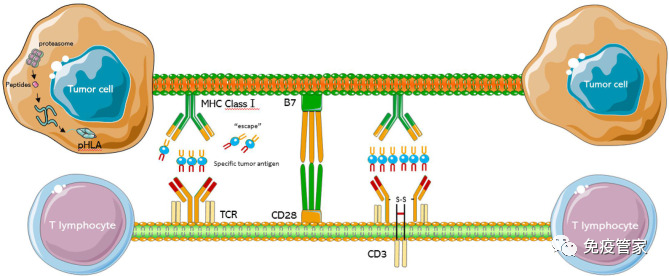
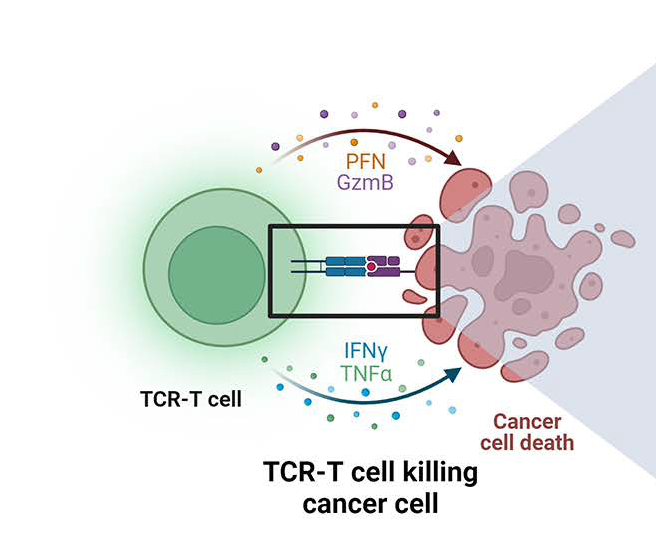
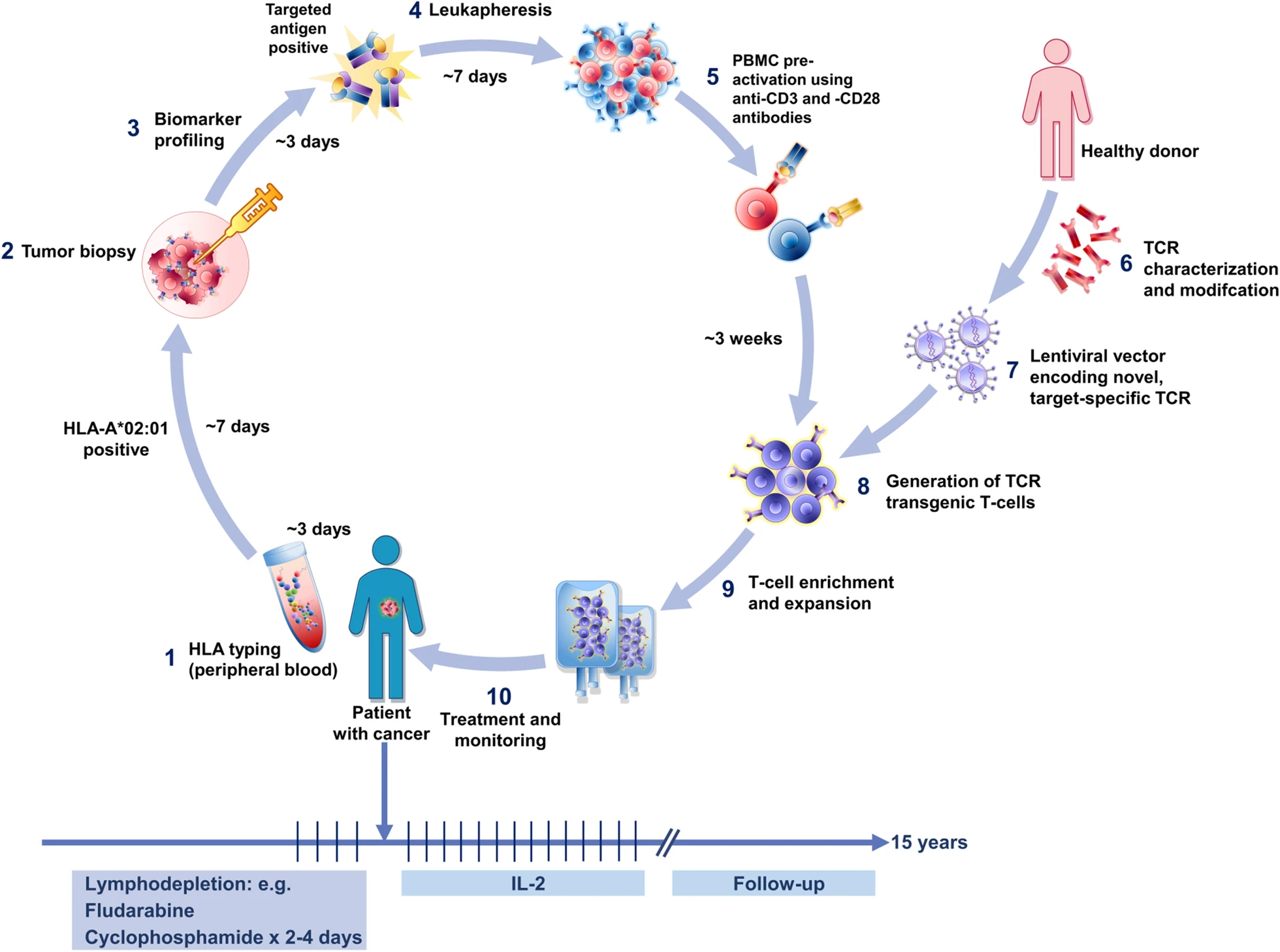
在我们的身体里,有一种非常重要的免疫细胞,叫做T细胞。它就像是身体里的“警察”,专门负责识别和清除那些“坏人”,比如癌细胞、病毒感染的细胞等。TCR-T细胞疗法,是将患者体内T细胞分离、纯化,利用基因工程技术通过病毒表达载体将特异性识别肿瘤抗原的TCR基因导入患者的T细胞中。转导成功的T细胞通过特异性的识别肿瘤细胞表面...