相关推荐

超90%的患者肿瘤缩小!CAR-T疗法不仅治血癌,卵巢癌也有效!晚期患者也能实现肿瘤消失
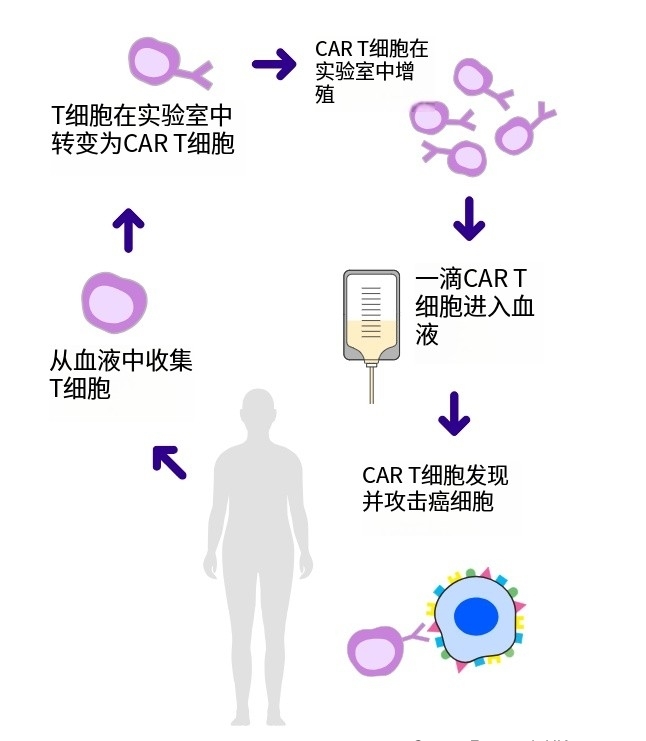
自2017年美国食品药品监督管理局(FDA)批准首个嵌合抗原受体T细胞(CAR-T)疗法以来,CAR-T治疗对于白血病、淋巴瘤和骨髓瘤等某些血癌具有革命性意义。
免疫管家 2025-08-26

惊!白血病女孩抗癌13年无复发!CAR-T疗法如何精准猎杀癌细胞?
近日,全球首位被CAR-T细胞疗法治愈的白血病儿童——Emily Whitehead在自己的社交媒体上发布了照片,并配文“13 years cancer free yesterday + celebrated being 20 today”。照片中的她笑容灿烂,而这简短的文字背后,是一场持续十余年的生命奇迹。
免疫管家 2025-06-24
CAR-T细胞产品纳基奥仑赛注射液亮相2025 ASCO和EHA
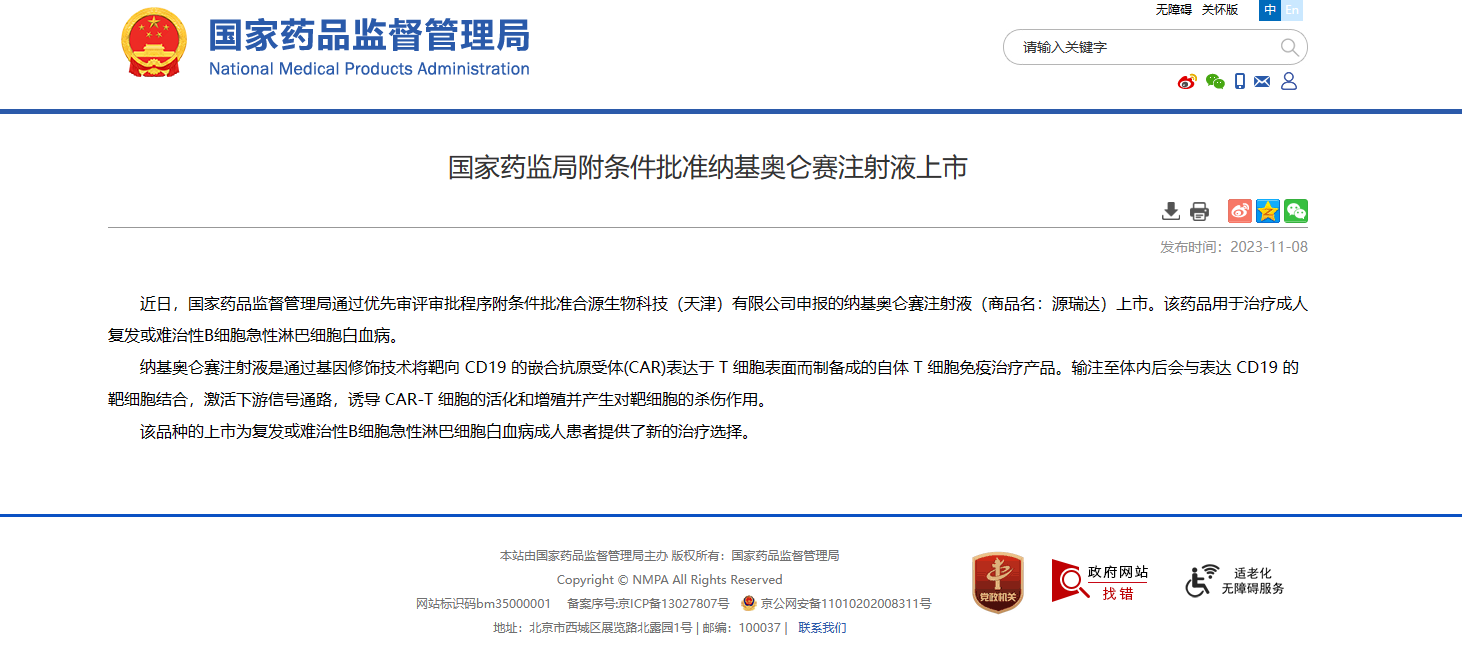
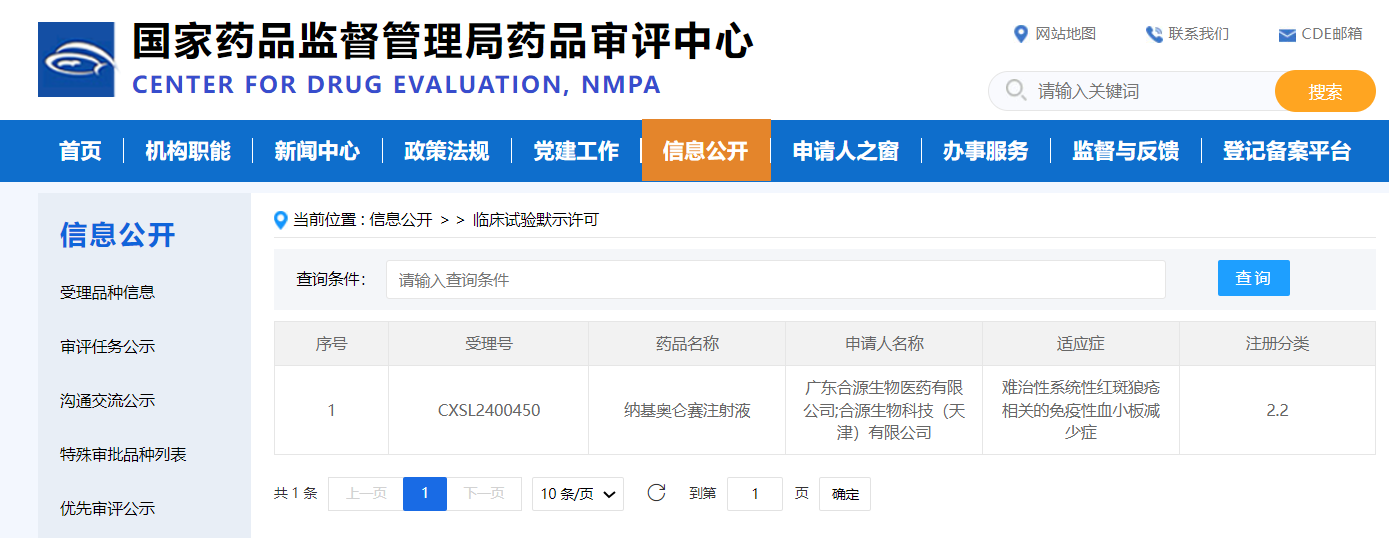
源瑞达®(纳基奥仑赛注射液,CNCT19,Inaticabtagene Autoleucel Injection)是具有自主知识产权的靶向CD19的CAR-T细胞治疗产品,拥有全球独特的CD19 scFv(HI19a)结构和国际领先的生产制造工艺,先后获得国家药品监督管理局三项新药临床试验许可(IND),用于治疗成人复...
免疫管家 2025-06-17