PF-07220060是一款 CDK4 选择性抑制剂,相较于 CDK4/6 抑制剂,对 CDK4 单靶点的选择性抑制有望减少 CDK6 靶点抑制所带来的中性粒细胞减少副作用。
在2024年欧洲肿瘤内科学会(ESMO)的乳腺癌大会上,1/2期试验(NCT04557449)的蕞新数据显示,此前对CDK4/6抑制剂耐药进展的乳腺癌患者,新型CDK4抑制剂PF-07220060联合内分泌治疗显示出良好的安全性,并在激素受体(HR)阳性、her2阴性的转移性乳腺癌患者中产生了强劲的反应率。
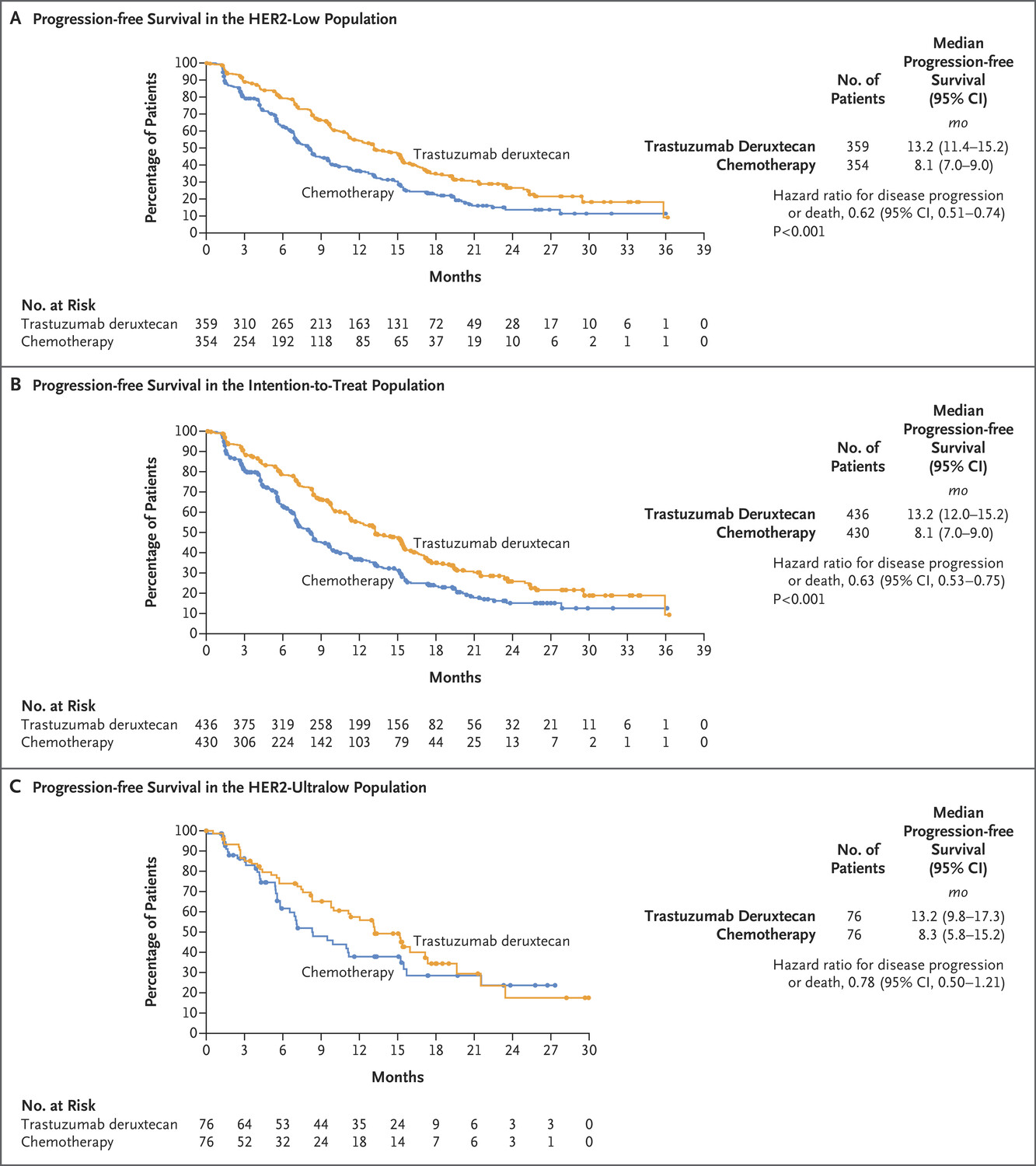
在2023年11月1日的数据截止日期,该组合分别在3.0%、21.2%、42.4%、18.2%和15.2%的患者中获得了完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)、疾病进展(PD)和非CR/非PD的最佳缓解(n = 33)。疾病控制率(DCR)为81.8%,中位无进展生存期为8.1个月。
这项首次在人体进行的2部分1/2a期试验的第一部分是剂量递增部分。在1A部分,旨在找到扩大PF-07220060的最大耐受剂量/推荐剂量,实体肿瘤患者,包括乳腺癌、非小细胞肺癌、前列腺癌、结直肠癌、脂肪肉瘤和其他CDK4/CCND1扩增的肿瘤。
PF-07220060 以每日两次剂量 300 mg 或 400 mg 联合来曲唑和氟维司群 (Faslodex) 进行评估,用于既往接受过 CDK4/6 抑制剂和内分泌治疗进展的 HR 阳性、HER2 阴性转移性乳腺癌患者。
在数据截止时,33名患者被纳入1B部分和1C部分组合。所有患者既往接受过 CDK4/6 抑制剂治疗;分别有72.7%和66.7%的患者既往接受过氟维司群或化疗。
在基线时有可测量疾病的患者(n = 25),中位随访时间为 13.0 个月,根据 RECIST v1.1 标准,确认的客观缓解率 (ORR) 为 32.0%,包括 1 例 CR 和 7 例 PR。中位缓解时间为3.6个月,临床获益率(CBR)为64.0%。
研究人员观察到已确认的客观反应,所有这些都是 PR,无论是否存在ESR1或PI3K通路突变。在ESR1突变患者(n=15)中,CR、PR、SD和PD发生率分别为0.0%、26.7%、60.0%和13.3%。ORR为26.7%,CBR为53.3%,DCR为86.7%。
在无ESR1突变(n=10)的患者中,CR、PR、SD和PD发生率分别为10.0%、30.0%、50.0%和10.0%。ORR为40.0%,CBR为80.0%,DCR为90.0%。
在具有 1 个或多个PIK3CA、AKT1或PTEN突变(n = 10)的患者中,CR、PR、SD 和 PD 发生率分别为 0.0%、40.0%、50.0% 和 10.0%。ORR为40.0%,CBR为70.0%,DCR为90.0%。
在没有PIK3CA、AKT1或PTEN突变(n=15)的患者中,CR、PR、SD和PD发生率分别为6.7%、20.0%、60.0%和13.3%。ORR为26.7%,CBR为60.0%,DCR为86.7%。
参考资料
Novel CDK4 Inhibitor Shows Activity and Safety in HR+/HER2– Metastatic Breast Cancer (onclive.com)