相关推荐
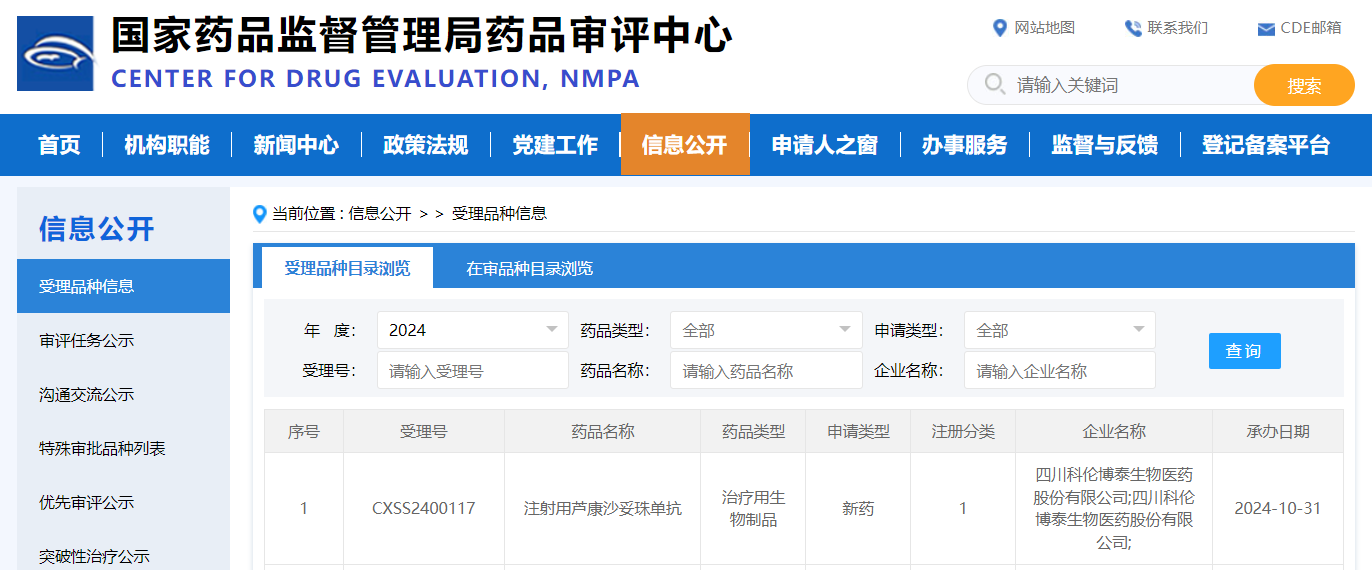
中位生存近5年!阿可替尼用于一线治疗慢性淋巴细胞白血病的新适应症获受理
8月28日,国家药品监督管理局药品审评中心(CDE)公示:阿斯利康申报的布鲁顿氏酪氨酸激酶(BTK)抑制剂acalabrutinib Maleate片(阿可替尼胶囊)新适应症申请已获得受理。推测适应症为一线治疗慢性淋巴细胞白血病(CLL)。
免疫管家 2024-09-05
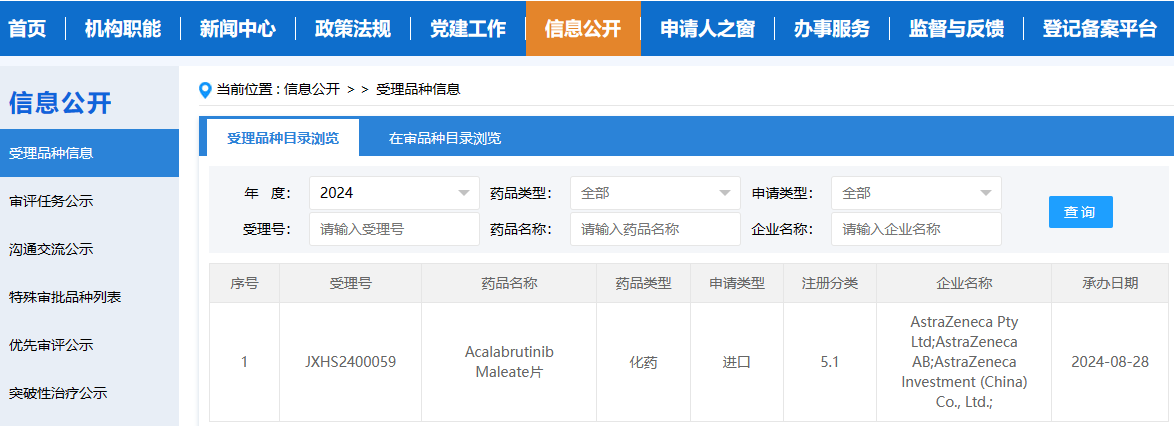
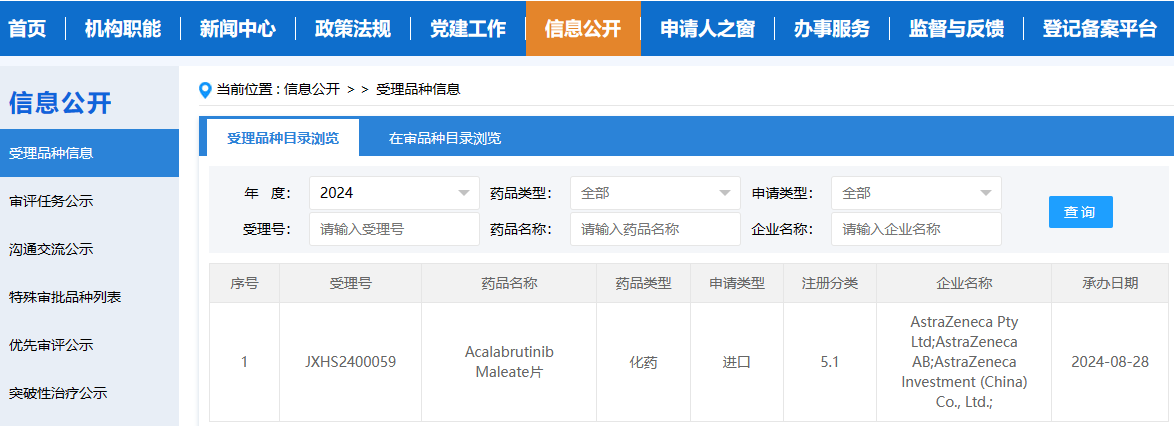
BTK抑制剂阿可替尼新适应症申请获受理
8月28日,国家药监局药品审评中心(CDE)显示:阿斯利康(AstraZeneca)申报的布鲁顿氏酪氨酸激酶(BTK)抑制剂acalabrutinib Maleate片(阿可替尼胶囊)新适应症申请已获得受理。
免疫管家 2024-08-31