
近年来,有研究已在阐明滋养层细胞表面抗原-2(Trop-2)在多种上皮癌中的信号传导机制方面取得了成功。大约40年前,Lipinski及其斯坦福大学同事报告了针对正常和恶性滋养层细胞单克隆抗体的产生。Trop-2就是其中一种被抗Trop-2单克隆抗体靶向的膜抗原之一。随后,Trop-2被确认为在大多数上皮癌中普遍存在的跨膜糖蛋白。

滋养层细胞表面抗原2(Trop-2)是一种跨上皮细胞膜表面的糖蛋白,在细胞自我更新、增殖和转化中发挥作用。Trop-2由TACSTD2基因编码,是一种35 kDa的蛋白质,由大的胞外域、单个跨膜域和一个短的胞内尾构成,其中胞内尾是其功能主导部分。
在生理条件下,Trop-2在胚胎发育、胎盘组织形成、胚胎植入、干细胞增殖和器官发育中起重要作用。在包括皮肤和口腔黏膜在内的多种正常上皮组织表面可检测到较低的Trop-2基础表达水平。Trop-2可促进肿瘤生长,其在许多类型的恶性上皮肿瘤中普遍存在过表达。Trop-2的过表达会加速癌细胞周期并驱动癌症生长。
Trop-2与癌症进展和转移密不可分,因为它作为癌症特征(包括细胞生长、增殖、迁移、侵袭和生存)的关键调节因子发挥作用。多种人类上皮癌细胞以Trop-2过表达为特征,包括乳腺癌、肺癌、尿路上皮癌、胃癌、结直肠癌、胰腺癌、前列腺癌、宫颈癌、头颈癌和卵巢癌。
由于Trop-2是几种实体瘤类型中临床上相关的细胞表面抗原,其在癌细胞上的过表达使其成为特定疗法靶向的理想候选物。一种靶向方法涉及使用抗体药物偶联物(ADC),这项技术在过去20年中彻底改变了癌症化疗的方法。如果需要TROP2检测,可以咨询康和源免疫之家(400-880-3716)。
体药物偶联物(ADC)是一种将单克隆抗体的靶向特异性与细胞毒性小分子药物通过连接子偶联而成的新型抗癌药物。简单来说,ADC药物就像是一个精准的“导弹”系统,单克隆抗体负责识别肿瘤细胞表面的特定抗原,就如同“导弹”的制导系统,能够准确地找到目标;
连接子确保细胞毒性小分子药物不会在血液循环中过早释放,避免对正常组织造成损伤;
而小分子细胞毒素则相当于“导弹”的战斗部,一旦连接子被切断,就可以发挥强大的杀伤作用,杀死肿瘤细胞。
芦康沙妥珠单抗(sac-TMT)是一款靶向TROP2的ADC药物。2024年11月,国家药监局批准其用于既往至少接受过2种系统治疗的三阴性乳腺癌成人患者。次年3月再次批准其用于EGFR基因突变阳性的局部晚期或转移性非鳞状非小细胞肺癌(NSCLC)成人患者。9月又批准用于经表皮生长因子受体(EGFR)酪氨酸激酶抑制剂(TKI)治疗后进展的EGFR基因突变阳性的局部晚期或转移性非鳞状非小细胞肺癌(NSCLC)成人患者。
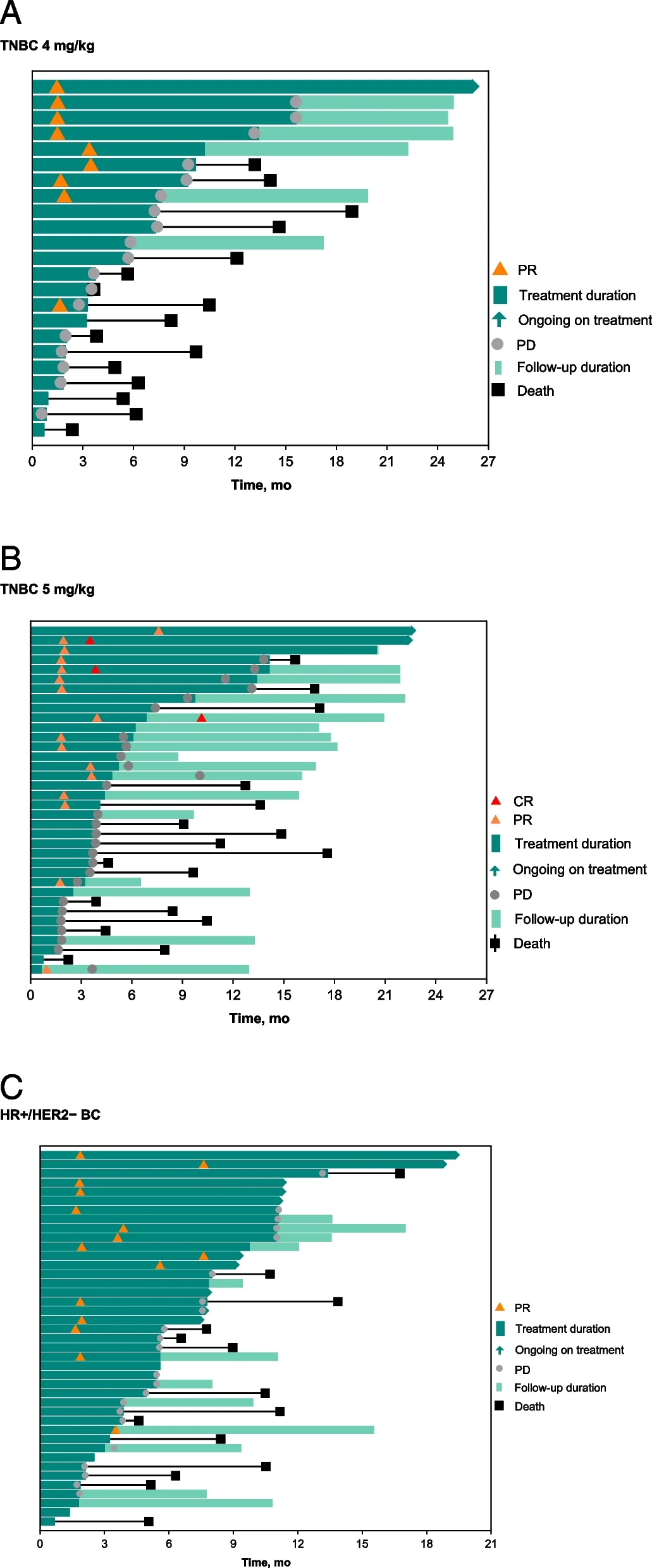
在Ⅰ/Ⅱ期KL264-01/MK-2870-001研究中,芦康沙妥珠单抗在标准疗法难治性的不可切除的局部晚期或转移性实体瘤患者中展现出良好的抗肿瘤活性:三阴性乳腺癌中客观缓解率为37%,中位缓解11.5个月,总生存期长达15.7个月。
幸运的是,目前芦康沙妥珠单抗正在国内开展临床研究。有意向接受芦康沙妥珠单抗治疗的患者可参与临床研究免费接受治疗。
1.经组织学证实诊断为子宫内膜癌或癌肉瘤。
2.存在BICR根据RECIST 1.1评估的影像学可评价病灶(可测量或不可测量)。
3.既往针对子宫内膜癌或癌肉瘤,接受过系统性铂类为基础的化疗和抗PD-1/抗PD-L1治疗(分别给药或联合治疗)。
1.患有神经内分泌肿瘤或子宫内膜肉瘤,包括间质肉瘤、平滑肌肉瘤、腺肉瘤或其他类型的单纯肉瘤。
2.有记录的重度干眼症、重度睑板腺疾病和/或睑缘炎或妨碍/延缓角膜愈合的角膜疾病史。
3.患有需要免疫抑制药物治疗的活动性炎症性肠病,或有炎症性肠病既往史。
4.在根治性治疗背景下完成铂类为基础治疗后>12个月子宫内膜癌或癌肉瘤复发,且在复发性疾病治疗中未接受任何额外的铂类为基础治疗。
5.既往接受过3线以上的子宫内膜癌或癌肉瘤治疗
临床试验对于传统疗法无效或疗效较差的患者来说,可能带来新的希望和治疗机会,并能大大减轻家庭经济负担。患者可通过参加临床试验来接受药物治疗,病历资料审核通过后可免费入组接受治疗。如果有需要或有兴趣了解临床试验的患者可以咨询康和源免疫之家医学部(400-880-3716)。
Trop-2已在几种实体恶性肿瘤中确立了自己作为具有临床意义的生物标志物的地位。其促进自我更新、增殖和细胞侵袭的能力使其成为包括ADC在内的靶向抗肿瘤疗法的理想候选靶点。戈沙妥珠单抗是首个获得美国食品药品监督管理局(FDA)批准用于治疗转移性三阴性乳腺癌的靶向Trop-2的ADC药物。随着更多药物的研究,未来这些药物将适用于广泛的肿瘤患者。
参考资料 1.https://www.xiahepublishing.com/2472-0712/ERHM-2022-00087 2.https://pmc.ncbi.nlm.nih.gov/articles/PMC8860310/ 3.https://www.onclive.com/view/trop-2-directed-antibody-drug-conjugates-for-the-treatment-of-solid-tumors 4.https://karger.com/pat/article/89/4/245/826136/Trophoblast-Cell-Surface-Antigen-2-Expression-in 5.https://www.onclive.com/view/expert-perspectives-on-trop-2-biomarker-expression-in-lung-cancer-and-the-potential-role-of-dato-dxd 6.https://www.onclive.com/view/defining-trop-2-and-antibody-drug-conjugates-in-nsclc 7.https://www.onclive.com/view/role-of-trop-2-as-an-actionable-biomarker-in-solid-tumors 如果您在阅读本文后仍有困惑,或需要帮助,可通过康和源免疫之家医学部(400-880-3716)获取专业指导。您可以通过添加以下微信方式联系我们。 康和源免疫之家-癌症患者的生命希望桥梁 康和源免疫之家作为肿瘤诊疗服务平台,始终秉持“以患者为中心”的理念。在肿瘤治疗领域,患者面临着巨大的身心压力和复杂的治疗选择,康和源免疫之家深知患者的需求和困境,致力于为患者提供全方位、个性化的服务。 为了实现这一目标,该平台整合了中国、美国、欧洲、日本、韩国等全球顶尖肿瘤专家资源。这些专家拥有丰富的临床经验和先进的治疗理念,能够为患者提供专业的诊断和治疗建议。同时,平台还与知名药企、创新药物研发机构建立了深度合作关系,这使得患者能够及时了解到前沿的抗癌药物和治疗技术,为治疗提供更多的选择。 国际专家会诊服务 肿瘤治疗具有复杂性和个体差异性,不同患者的病情和身体状况各不相同,因此需要个性化的治疗方案。康和源免疫之家通过国际专家会诊服务,可协调中美欧日韩等多国权威肿瘤专家,针对癌症开展跨国联合诊疗。 对于那些需要第二诊疗意见的患者来说,国际专家会诊可以提供不同的视角和建议,帮助患者更全面地了解自己的病情和治疗方案。而对于寻求海外先进治疗方案的患者,平台的专业团队能够帮助他们获取国际前沿治疗指南,为患者制定更加科学、合理的治疗计划。 临床试验 作为连接患者与创新疗法的纽带,康和源免疫之家与全球领先药企及研发机构保持战略合作,持续提供涉及PD-1/L1抑制剂、CAR-T细胞治疗、ADC药物等领域的临床试验项目。这些临床试验项目代表了当前癌症治疗的前沿进展和研究方向,为患者提供了接触新型抗癌药物和治疗技术的机会。 康和源免疫之家团队会根据患者的病情阶段、基因检测结果和治疗史,精准匹配适合的临床试验机会。这不仅提高了患者参与临床试验的成功率,也确保了患者能够接受更加适合自己的治疗。在康和源免疫之家,每个生命都被视为值得更好的医疗选择,无论是寻求国际顶尖专家的诊疗建议,还是尝试突破性的临床试验,平台都将竭诚为患者提供专业、可靠的全方位支持。让我们携手,在抗击肿瘤的征程上走得更远。 END 如果您或您身边的人正在遭受癌症的困扰,不妨拨打咨询电话400-880-3716,登录官网 https://www.myimm.net/或关注微信公众号“康和源免疫之家”(头条、知乎、百度、搜狐等自媒体同名),了解更多关于临床试验和肿瘤诊疗服务的信息。
相关推荐
随便看看
- 精准检测指导精准治疗:TROP-2 ADC芦康沙妥珠单抗让55%肺癌患者肿瘤缩小,乳腺癌疗效提升近4倍
- 71%肺癌患者肿瘤缩小!HER2靶向治疗新时代,胃癌/肺癌/乳腺癌全覆盖!这些患者都可能受益
- 甲胎蛋白 (AFP)
- 13岁少年、剧痛难眠,面对巨大肿瘤,手术还是等待?基因检测发现NTRK融合,为他迎来转机
- 美国FDA加速批准新疗法,BRAF V600E突变结直肠癌患者的救命稻草
- TRK抑制剂佐来曲替尼纳入儿童肿瘤药“星光计划”
- 芭比Q了,火烤癌细胞,癌细胞真的能被热死吗?
- 71%患者肿瘤显著缩小!戈来雷塞联合AST24082拟纳入突破性治疗品种,靶向耐药有了新打法
- 肿瘤缩小91%!广谱抗癌药拉罗替尼让NTRK基因融合患者重获新生
- 不再是“老大难”!肺癌EGFR 20ins、L858R等难治突变迎来高效新药











