热门推荐
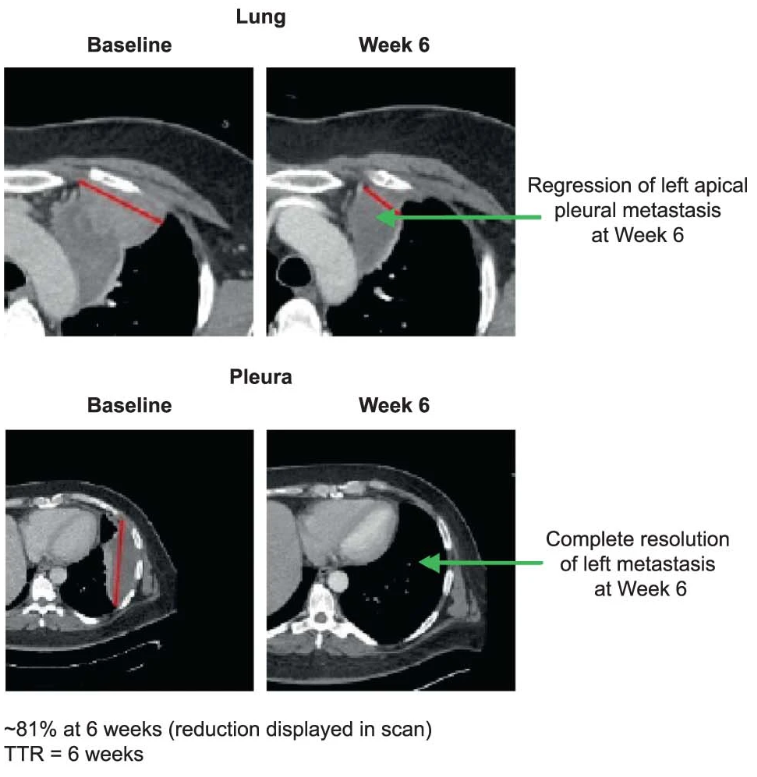
- 精 疾病控制率高达90%!TCR-T细胞横扫黑色素瘤、宫颈癌、肉瘤、肝癌等实体瘤,肿瘤缩小81%!
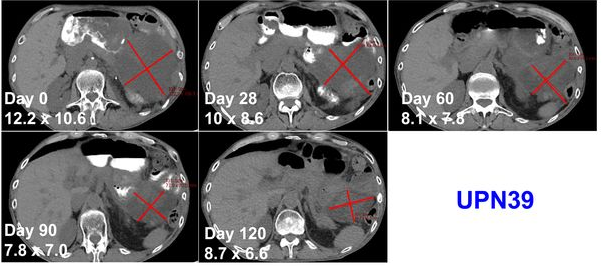
- 精 首款用于治疗实体瘤的TCR-T细胞疗法获批在即!非小细胞肺癌治疗43天肿瘤缩小
- 精 肿瘤新型杀伤武器-TCR-T细胞疗法在肝细胞癌、胰腺癌、卵巢癌、尿路上皮癌等癌种中前景广阔
- 精 87%患者肿瘤缩小!TCR-T疗法惠及滑膜肉瘤、黑色素瘤等实体瘤!
- 精 87% 患者肿瘤缩小!TCR-T疗法IMA203用以治疗经治转移性黑色素瘤患者的最新数据公布
- 精 治疗8个月约25个肺部肿瘤完全消退!TCR-T治疗在宫颈癌等多种HPV相关肿瘤中表现优异
- 精 TCR-T狙击手已到位,狙击宫颈癌,肝癌等多款实体瘤!
- 精 肝癌晚期怎么办?TCR-T和CAR-T细胞疗法迎来新希望
- 精 与CAR-T媲美的细胞疗法,看“显眼包”TCR-T如何攻击癌细胞?
- 精 攻克实体瘤哪家强,细胞疗法找TCRT
- 精 TCR-T细胞疗法针对实体瘤患者的临床试验开始了
- 精 国内TCR-T细胞疗法获批临床
资讯列表
1月13日,Adaptimmune Therapeutics宣布Letetresgene autoleucel(Lete-cel)已被美国食品药品监督管理局(FDA)授予突破性疗法认定,用于治疗既往接受过蒽环类药物治疗的不可切除或转移性粘液样/圆细胞脂肪肉瘤(MRCLS)患者,这些患者HLA-a*02:01、HLA-a...
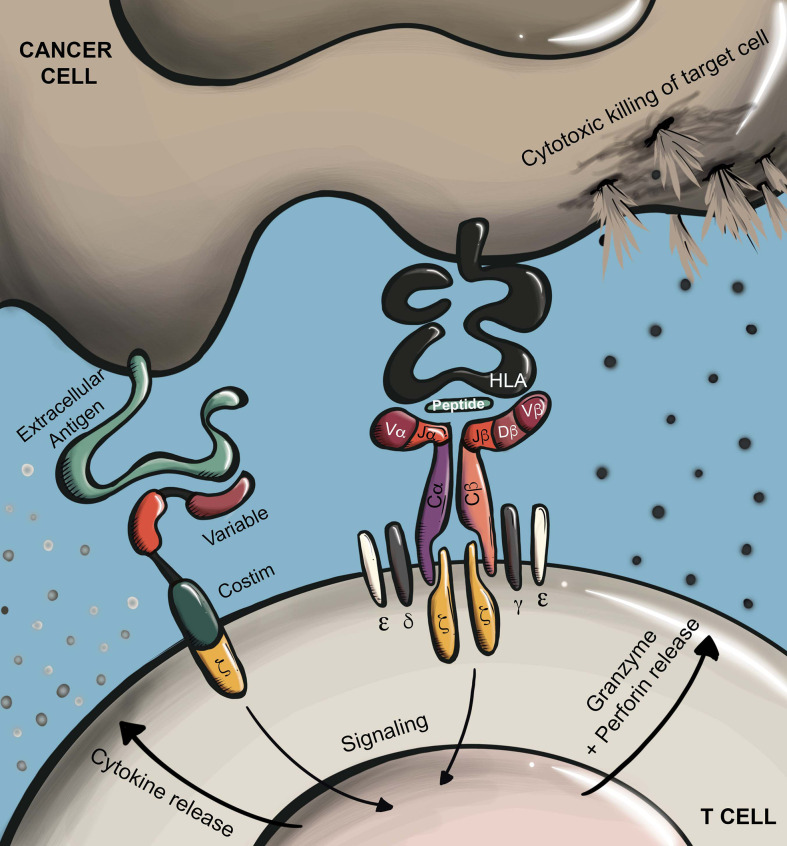
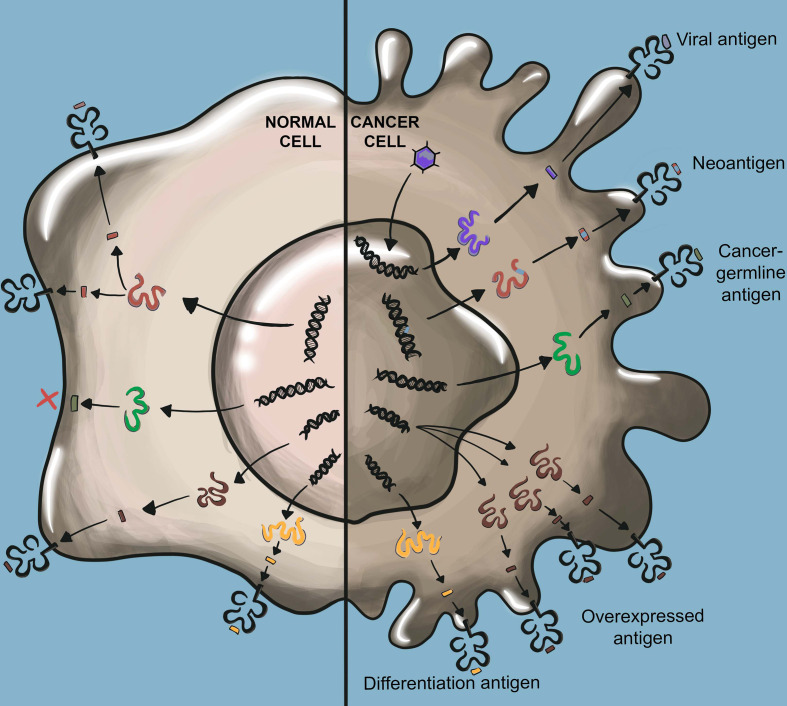
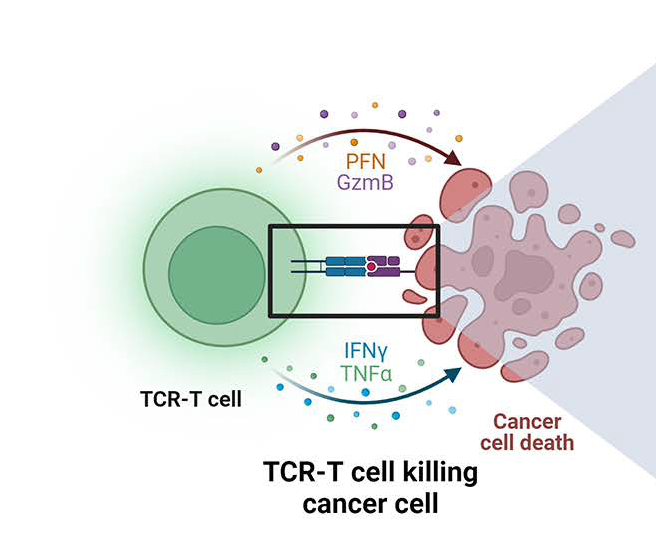
T细胞受体工程化T细胞疗法(TCR-T)通过基因编辑技术将能够识别特定癌症抗原的TCR基因导入患者的T细胞中,使这些T细胞发挥特异性识别和杀伤肿瘤细胞的作用。
1月13日,Adaptimmune Therapeutics宣布Letetresgene autoleucel (Lete-cel)已被美国 FDA 授予突破性疗法认定,用于治疗既往接受过蒽环类药物治疗的不可切除或转移性粘液样/圆细胞脂肪肉瘤(MRCLS)患者,这些患者HLA-a*02:01、HLA-a*2:05或HL...
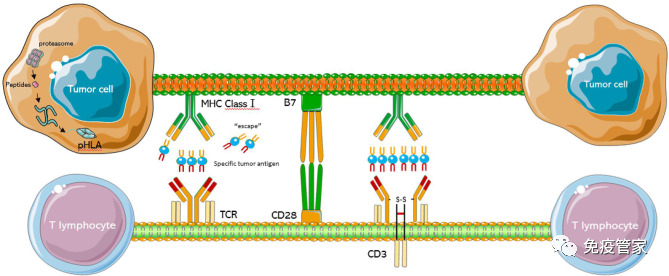
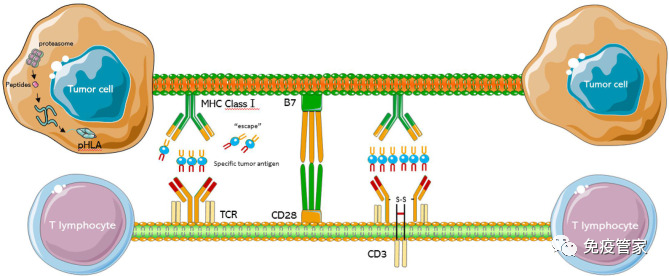
过继细胞疗法是癌症免疫疗法最有前途的领域之一,改造患者自身的 T 细胞以增强身体的天然抗肿瘤免疫反应,以对抗恶性肿瘤。但是如早期CAR-T研究所示,细胞因子释放综合征(CRS)的风险增加。为了提高过继性 T 细胞疗法的安全性和有效性,已经引入了使用 T 细胞受体(TCR)代替 CAR-T 来降低 CRS 风险的方法。
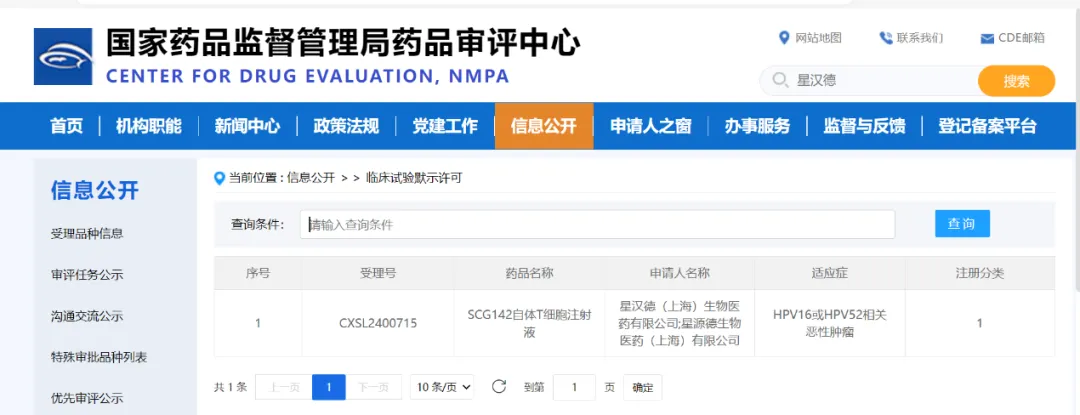
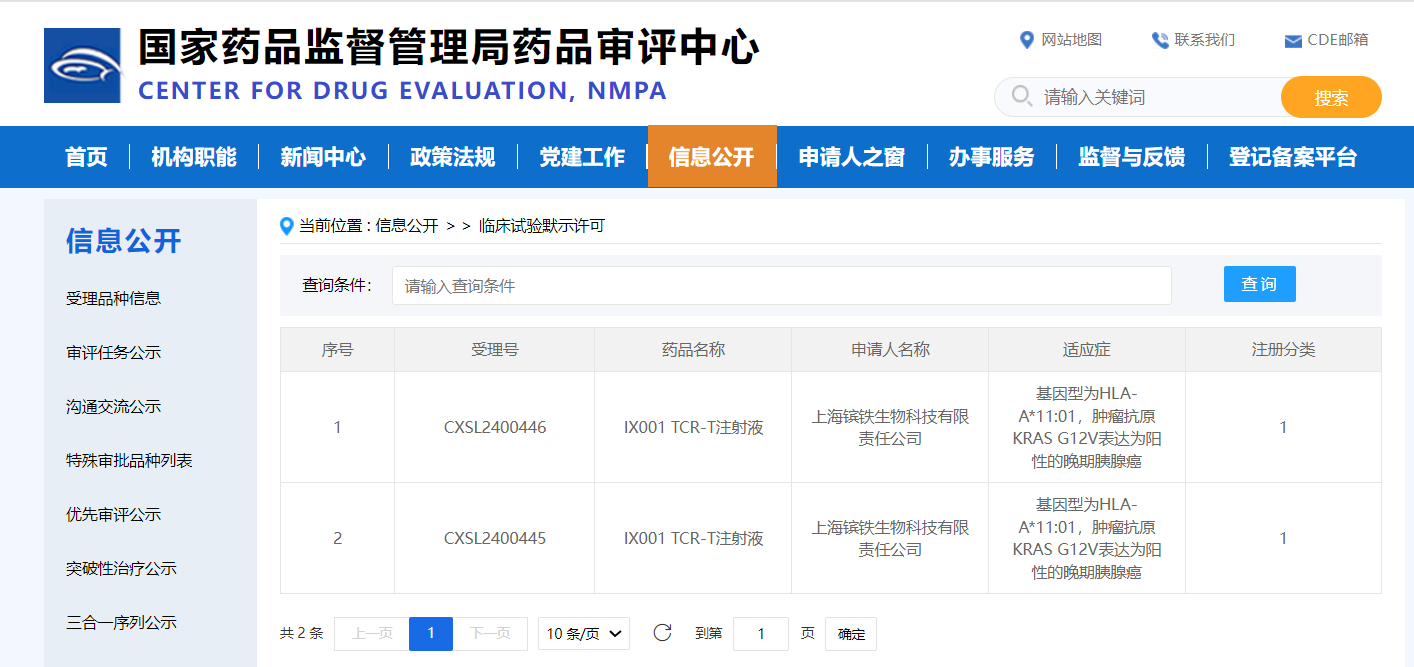
2025年1月2日,星汉德生物宣布,国家药品监督管理局药品审评中心(CDE)已批准其全新一代人乳头瘤病毒(HPV)特异性T细胞受体(TCR)工程化T细胞治疗产品-SCG142的新药临床试验(IND)申请,用于治疗HPV感染相关的恶性肿瘤,包括宫颈癌、口咽癌、头颈癌、阴道癌、外阴癌和阴茎癌等。
1月2日,星汉德生物(SCG)宣布,国家药品监督管理局药品审评中心(NMPA)已批准其全新一代人乳头瘤病毒(HPV)特异性T细胞受体(TCR)工程化T细胞治—SCG142的新药临床试验(IND)申请,用于治疗HPV感染相关的恶性肿瘤,包括宫颈癌、口咽癌、头颈癌、阴道癌、外阴癌和阴茎癌等。
CAR-T是当下研发热度非常高的癌症免疫治疗方法,但是CAR-T细胞治疗在实体瘤中缺乏特异性抗原使得很难在不伤害健康组织的情况下靶向肿瘤细胞,越来越多的患者期待新型的治疗方式。
近年来,针对T细胞的CAR-T、TCR-T细胞疗法逐渐被大众熟知。其中工程化T细胞疗法(TCR-T)通过基因工程技术,将能够识别特定癌症抗原的TCR基因导入患者的T细胞中,使这些T细胞发挥特异性识别和杀伤肿瘤细胞的作用,以此来达到抗癌的目的。