热门推荐
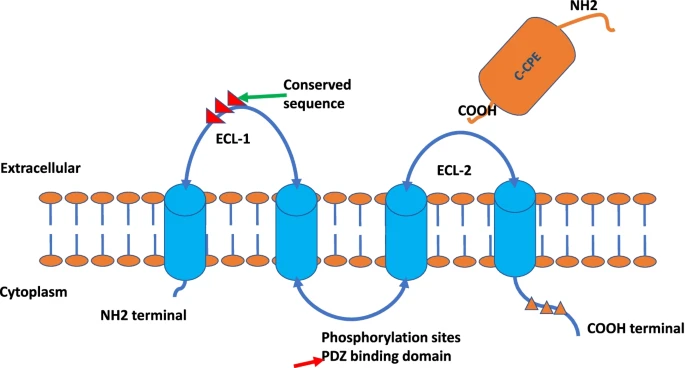
- 精 日本上市佐妥昔单抗(Zolbetuximab),claudin (CLDN)18.2阳性胃癌患者迎来新药
- 精 疾病控制率高达90.9%!KRAS G12C抑制剂出击结直肠癌、非小细胞肺癌!
- 精 重磅!“治愈”肺癌更进一步!ALK抑制剂阿来替尼无病生存率高达93.8%!
- 精 85%患者的病情得到控制!KRAS G12C突变的患者有前景的治疗选择
- 精 HER2阳性实体瘤患者命运将改写!DS-8201再获FDA批准,不限癌种!
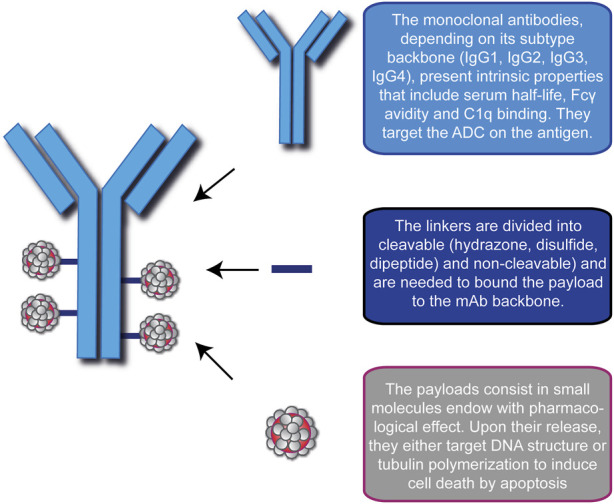
- 精 惊喜!无侵袭性癌生存率达到88.3%,一文读懂15款抗体偶联ADC药物
- 精 复发风险降低60%!特瑞普利单抗注射液再填适应症,我国首个、全球第二个获批的肺癌围手术期疗法
- 精 好消息!21款抗肿瘤药物纳入医保目录!但CAR-T产品无缘此次医保名单!
- 精 NTRK融合让众多实体瘤战栗,成为击败肿瘤的重磅武器
- 精 奥布替尼(Orelabrutinib)广受认可,让更多血液系统肿瘤患者获益
- 精 首款RET抑制剂普拉替尼给非小细胞肺癌患者带来希望
- 精 肿瘤和免疫的关系如何?CAR-T细胞疗法全球上市有9款
- 精 收藏 | 不能错过的胃癌的药物治疗大全!
- 精 KRAS基因靶点药物不间断研究中
- 精 仑伐替尼一种重要的靶向药
- 精 “不完美心动”——干细胞叫嚣“心衰”
- 精 伏美替尼 (Furmonertinib)第三代EGFR-TKI强势来袭
- 精 一文教会你BRCA突变和PAPR抑制剂的关系
- 精 国家药监局批准三款新药上市!!!攻克癌症不再天方夜谭!
- 精 中国首款自主研发的CAR-T细胞治疗伊基奥伦赛注射液获批上市
- 精 培美曲塞
资讯列表
TCR-T是什么细胞TCR-T疗法也是过继细胞转移疗法(ACT)的一种,通过筛选和鉴定能特异性结合靶抗原的TCR序列,利用基因工程改造来自患者外周血的T细胞,然后将改造后的T细胞回输至患者体内,使其能特异性识别并杀伤表达抗原的肿瘤细胞,从而达到治疗肿瘤的目的。是近年来癌症治疗新方法的焦点,这种新型的免疫基因疗法,可以让...
6月10日,诺华公司宣布其双靶向联合治疗药物泰菲乐®(甲磺酸达拉非尼胶囊)联合迈吉宁®(曲美替尼片)获国家药品监督管理局批准新增适应症,用于治疗BRAF V600E突变阳性、放射性碘难治或不适用、且血管内皮生长因子酪氨酸激酶抑制剂(VEGFR-TKI)治疗失败的局部晚期或转移性分化型甲状腺癌成人患者。这是泰菲乐®联合迈...
近日,在美国芝加哥举行的第62届美国临床肿瘤学会(ASCO)年会上,浙江省肿瘤医院宋正波教授以口头报告形式,首次公布了珃诺生物自主研发的高选择性、口服KRAS G12D小分子抑制剂RNK08954的单药治疗I期临床数据。
近日,在美国芝加哥举行的第62届美国临床肿瘤学会(ASCO)年会上,浙江省肿瘤医院宋正波教授以口头报告形式,首次公布了珃诺生物自主研发的高选择性、口服KRAS G12D小分子抑制剂RNK08954的单药治疗I期临床数据。
在2026年美国临床肿瘤学会(ASCO)年会上,中国药企迈威生物公布了一项关于新型ADC药物-9MW2821(Bulumtatug fuvedotin,BFv)联合特瑞普利单抗的研究数据。
6月4日,国家药品监督管理局(NMPA)批准江苏威凯尔医药申报的1类创新药安瑞曲替尼胶囊(商品名:维迈妥®)上市,用于治疗携带NTRK融合基因的成人和12岁以上青少年实体瘤患者。
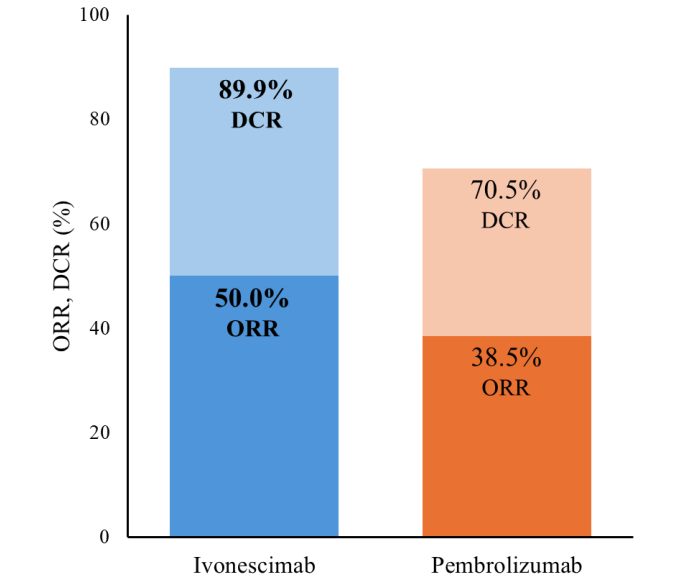
2026年美国临床肿瘤学会(ASCO)年会上公布了宜明昂科自主研发的VEGF×PD-L1双靶点药物珀维拉芙普α(IMM2510)I期临床研究数据。
6月4日,国家药品监督管理局(NMPA)批准威凯尔医药自主研发的1类创新药-维迈妥®(通用名:安瑞曲替尼/Eratrectinib,研发代码:VC004)上市,用于治疗携带NTRK融合基因的成人和12岁以上青少年实体瘤患者。该药是全球第三款新一代TRK抑制剂。