热门推荐
- 精 日本上市佐妥昔单抗(Zolbetuximab),claudin (CLDN)18.2阳性胃癌患者迎来新药
- 精 疾病控制率高达90.9%!KRAS G12C抑制剂出击结直肠癌、非小细胞肺癌!
- 精 重磅!“治愈”肺癌更进一步!ALK抑制剂阿来替尼无病生存率高达93.8%!
- 精 85%患者的病情得到控制!KRAS G12C突变的患者有前景的治疗选择
- 精 HER2阳性实体瘤患者命运将改写!DS-8201再获FDA批准,不限癌种!
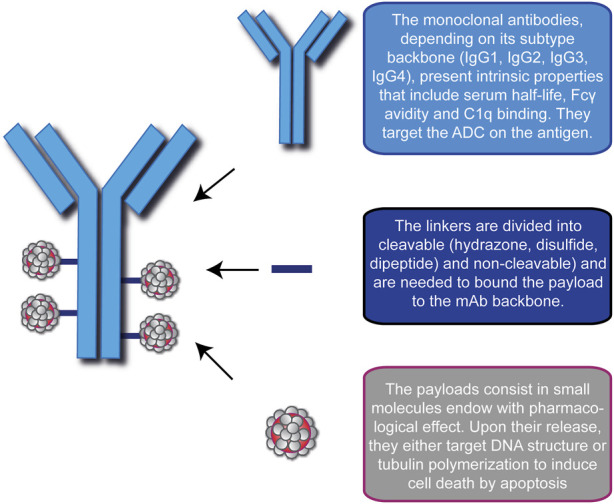
- 精 惊喜!无侵袭性癌生存率达到88.3%,一文读懂15款抗体偶联ADC药物
- 精 复发风险降低60%!特瑞普利单抗注射液再填适应症,我国首个、全球第二个获批的肺癌围手术期疗法
- 精 好消息!21款抗肿瘤药物纳入医保目录!但CAR-T产品无缘此次医保名单!
- 精 NTRK融合让众多实体瘤战栗,成为击败肿瘤的重磅武器
- 精 奥布替尼(Orelabrutinib)广受认可,让更多血液系统肿瘤患者获益
- 精 首款RET抑制剂普拉替尼给非小细胞肺癌患者带来希望
- 精 肿瘤和免疫的关系如何?CAR-T细胞疗法全球上市有9款
- 精 收藏 | 不能错过的胃癌的药物治疗大全!
- 精 KRAS基因靶点药物不间断研究中
- 精 仑伐替尼一种重要的靶向药
- 精 “不完美心动”——干细胞叫嚣“心衰”
- 精 伏美替尼 (Furmonertinib)第三代EGFR-TKI强势来袭
- 精 一文教会你BRCA突变和PAPR抑制剂的关系
- 精 国家药监局批准三款新药上市!!!攻克癌症不再天方夜谭!
- 精 中国首款自主研发的CAR-T细胞治疗伊基奥伦赛注射液获批上市
- 精 培美曲塞
资讯列表
3月31日,国家药品监督管理局药品审评中心(CDE)显示:Amivantamab注射液(皮下注射)拟纳入突破性治疗,适用于作为单药治疗用于含铂化疗和PD-(L)1抑制剂治疗期间或治疗后疾病进展的HPV无关复发性或转移性头颈部鳞状细胞癌(R/M HNSCC)成人患者。
3月31日,国家药品监督管理局药品审评中心(CDE)显示:劲方医药的GFH375片拟纳入突破性治疗,用于至少接受过一种系统性治疗并具有KRAS G12D突变的转移性胰腺癌。
4月1日,荣昌生物宣布其自主研发的双抗ADC药物RC288,正式获得国家药品监督管理局药品审评中心(CDE)批准,将开展单药治疗局部晚期不可切除或转移性恶性实体肿瘤的Ⅰ/Ⅱa期临床试验。
3月25日,《新英格兰医学杂志》(NEJM)在线发表一项评估KRAS G12D蛋白靶向降解剂setidegrasib对非小细胞肺癌(NSCLC)和胰腺导管腺癌患者的安全性与初步疗效的1期临床试验结果。
3月31日,国家药品监督管理局药品审评中心(CDE)显示:注射用芦康沙妥珠单抗拟纳入优先审评,用于联合帕博利珠单抗用于经国家药品监督管理局批准的检测评估为PD-L1肿瘤比例分数(TPS)≥ 1%的表皮生长因子受体(EGFR)基因突变阴性和间变性淋巴瘤激酶(ALK)阴性的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者...
2026年3月25日,美国食品药品监督管理局批准relacorilant (Lifyorli)一种糖皮质激素受体拮抗剂,联合白蛋白结合型紫杉醇,用于治疗成人铂类耐药性上皮性卵巢癌、输卵管癌或原发性腹膜癌患者,这些患者既往接受过1至3种全身治疗方案,且其中至少一种方案包含贝伐珠单抗。
近日,中国国家药品监督管理局批准了靶向药物优赫得®(注射用德曲妥珠单抗)的一项全新适应症,用于HER2阳性II期(高危)或III期乳腺癌成人患者的新辅助治疗。
近日,在2026年欧洲肺癌大会(ELCC 2026)上公布了君实生物自主研发的特瑞普利单抗皮下注射液(产品代号:JS001sc)对比特瑞普利单抗静脉注射液(产品代号:JS001)联合化疗一线治疗复发或转移性非鳞状非小细胞肺癌(NSCLC)的Ⅲ期临床研究(研究代号:JS001sc-002-III-NSCLC)结果。