相关推荐

硫酸索西美雷塞片在国内获批上市
2月28日,国家药品监督管理局(NMPA)批准硫酸索西美雷塞片(商品名:济乐美)上市,该药适用于至少接受过一种系统性治疗的鼠类肉瘤病毒癌基因(KRAS)G12C突变型的晚期非小细胞肺癌(NSCLC)成人患者。
免疫管家 2026-03-02
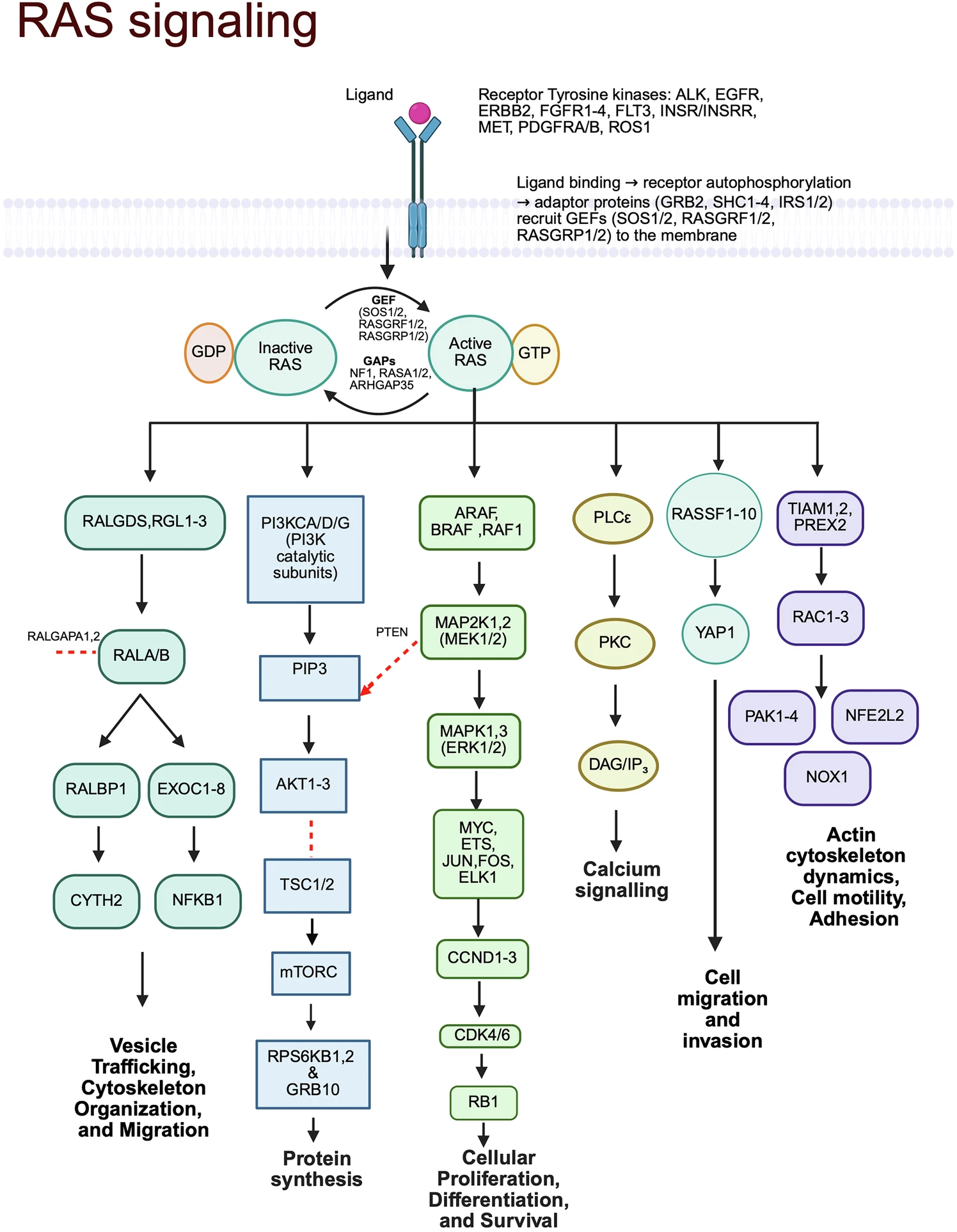
KRAS突变≠无药可医!40年“不可成药”魔咒,已被打破,曾经无药可医,如今多药可选!
曾几何时,KRAS突变在肺癌治疗领域如同一个令人绝望的标签——它意味着传统靶向药无效、化疗效果有限、预后普遍不佳。但2026年的今天,KRAS突变肺癌的治疗格局已经发生了翻天覆地的变化。从“不可成药”的魔咒被打破,到国产创新药纳入医保,再到联合治疗方案将疗效推向新高,KRAS突变患者正迎来前所未有的治疗希望。
免疫管家 2026-02-28

MK-1084片拟纳入突破性治疗
2月13日,国家药品监督管理局药品审评中心(CDE)显示:MK-1084片拟纳入突破性治疗,联合帕博利珠单抗用于一线治疗PD-L1 TPS ≥50%且有KRAS G12C突变的NSCLC患者。
免疫管家 2026-02-13
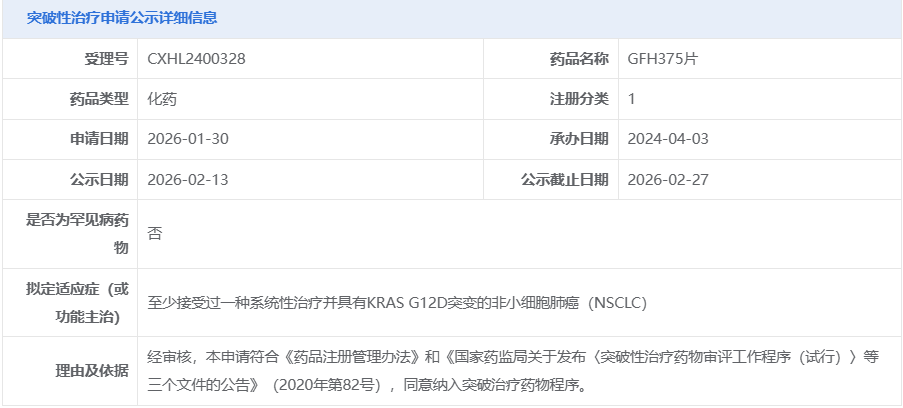
GFH375片拟纳入突破性治疗
2月13日,国家药品监督管理局药品审评中心(CDE)显示:GFH375片拟纳入突破性治疗,用于至少接受过一种系统性治疗并具有KRAS G12D突变的非小细胞肺癌(NSCLC)。
免疫管家 2026-02-13
疾病控制率93.3%!针对常见的KRAS G12D突变胰腺癌靶向药,已进入突破性治疗通道
2026年1月29日,国家药品监督管理局药品审评中心公示,恒瑞医药申请的HRS-4642注射液拟纳入突破性治疗品种,用于携带KRAS G12D突变的晚期或转移性胰腺癌的一线治疗。
免疫管家 2026-02-04

HRS-4642注射液拟纳入突破性治疗
1月29日,国家药品监督管理局药品审评中心(CDE)显示:恒瑞医药申请的HRS-4642注射液拟纳入突破性治疗,用于联合吉西他滨和紫杉醇(白蛋白结合型)用于携带KRAS G12D突变的晚期或转移性胰腺癌的一线治疗。
免疫管家 2026-01-30
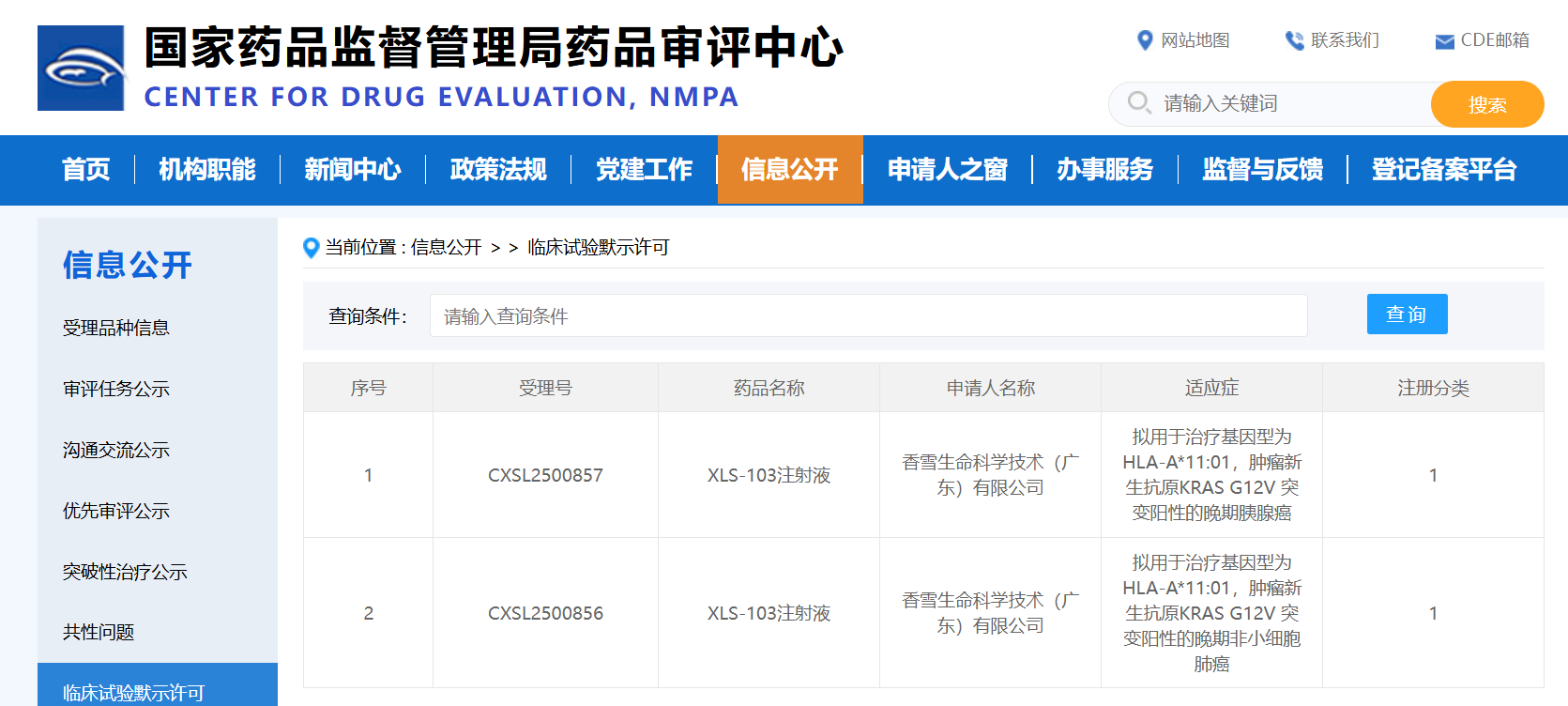
TCR-T细胞治疗产品“XLS-103注射液”新药临床试验申请获批
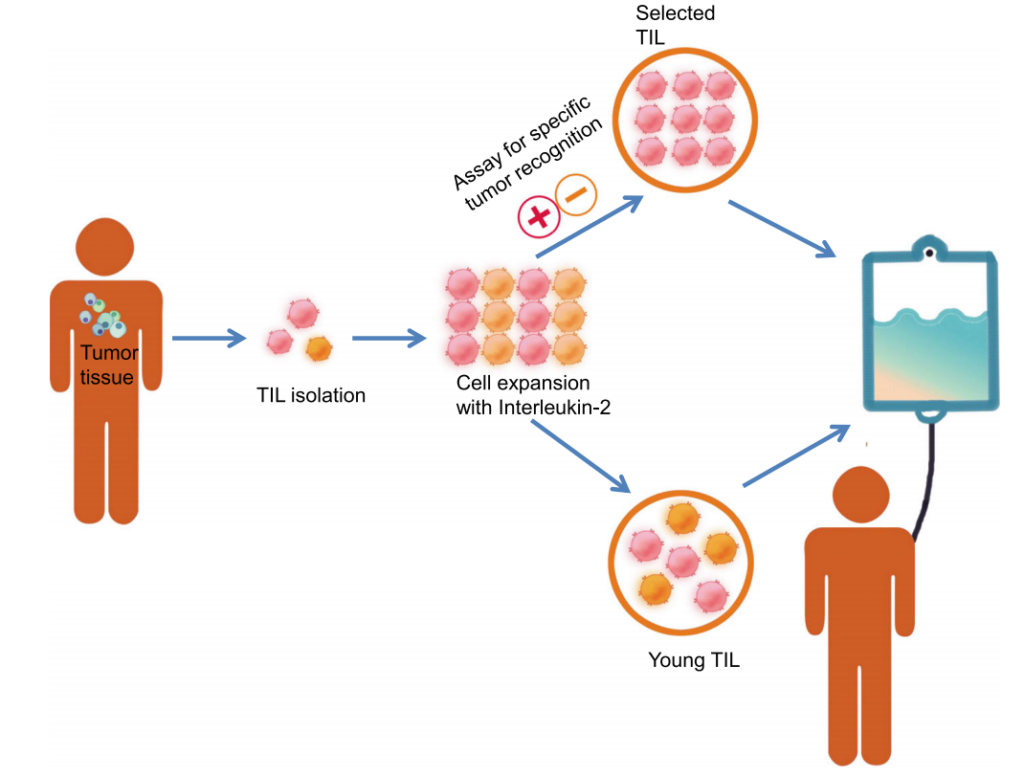
12月22日,香雪生命科学宣布其自主研发的高亲和力TCR-T细胞治疗产品“XLS-103注射液”新药临床试验申请(IND)获得国家药品监督管理局药品评审中心(CDE)批准,用于治疗基因型为HLA-A*11:01,肿瘤新生抗原KRAS G12V突变阳性的晚期非小细胞肺癌以及基因型为HLA-A*11:01,肿瘤新生抗原KR...
免疫管家 2025-12-24

KRAS G12C抑制剂格索雷塞用于KRAS G12C突变的晚期胰腺癌患者的临床数据公布
12月4日,国际权威期刊《英国癌症杂志》(British Journal of Cancer)发表了KRAS G12C抑制剂格索雷塞(D-1553,安方宁®)用于携带KRAS G12C突变的晚期胰腺癌患者的报告数据。
免疫管家 2025-12-12

KRAS G12C 抑制剂戈来雷塞临床试验结果发表于《柳叶刀胃肠与肝病学》
12月1日,KRAS G12C 抑制剂戈来雷塞(glecirasib,JAB-21822)的关键临床试验结果正式发表于国际顶级医学期刊《柳叶刀胃肠与肝病学》。
免疫管家 2025-12-08

KRAS G12D抑制剂ABSK141新药临床试验申请获得美国FDA批准
12月1日,和誉生物宣布其在研的口服、高活性、高选择性小分子KRAS G12D抑制剂ABSK141用于治疗携带KRAS G12D突变的晚期实体瘤患者的新药临床试验(IND)申请已获得美国食品药品监督管理局(FDA)批准。
免疫管家 2025-12-02