热门推荐
- 精 日本上市佐妥昔单抗(Zolbetuximab),claudin (CLDN)18.2阳性胃癌患者迎来新药
- 精 疾病控制率高达90.9%!KRAS G12C抑制剂出击结直肠癌、非小细胞肺癌!
- 精 重磅!“治愈”肺癌更进一步!ALK抑制剂阿来替尼无病生存率高达93.8%!
- 精 85%患者的病情得到控制!KRAS G12C突变的患者有前景的治疗选择
- 精 HER2阳性实体瘤患者命运将改写!DS-8201再获FDA批准,不限癌种!
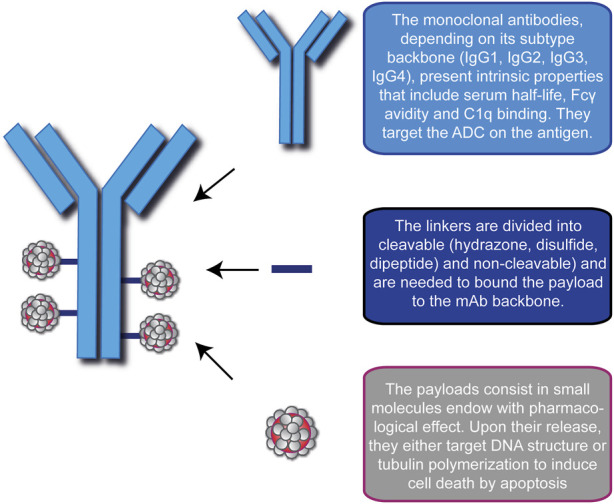
- 精 惊喜!无侵袭性癌生存率达到88.3%,一文读懂15款抗体偶联ADC药物
- 精 复发风险降低60%!特瑞普利单抗注射液再填适应症,我国首个、全球第二个获批的肺癌围手术期疗法
- 精 好消息!21款抗肿瘤药物纳入医保目录!但CAR-T产品无缘此次医保名单!
- 精 NTRK融合让众多实体瘤战栗,成为击败肿瘤的重磅武器
- 精 奥布替尼(Orelabrutinib)广受认可,让更多血液系统肿瘤患者获益
- 精 首款RET抑制剂普拉替尼给非小细胞肺癌患者带来希望
- 精 肿瘤和免疫的关系如何?CAR-T细胞疗法全球上市有9款
- 精 收藏 | 不能错过的胃癌的药物治疗大全!
- 精 KRAS基因靶点药物不间断研究中
- 精 仑伐替尼一种重要的靶向药
- 精 “不完美心动”——干细胞叫嚣“心衰”
- 精 伏美替尼 (Furmonertinib)第三代EGFR-TKI强势来袭
- 精 一文教会你BRCA突变和PAPR抑制剂的关系
- 精 国家药监局批准三款新药上市!!!攻克癌症不再天方夜谭!
- 精 中国首款自主研发的CAR-T细胞治疗伊基奥伦赛注射液获批上市
- 精 培美曲塞
资讯列表
12月9日,第一三共宣布美国食品药品监督管理局(FDA)授予Datopotamab deruxtecan (Dato-DXd)突破性疗法认定,用于治疗接受EGFR 酪氨酸激酶抑制剂(TKI)和铂类化疗期间或之后出现疾病进展的局部晚期或转移性表皮生长因子受体突变(EGFR 突变)非小细胞肺癌(NSCLC)成人患者。
12月13日,康宁杰瑞宣布在2024年欧洲肿瘤内科学会免疫肿瘤学(ESMO IO)大会上公布PD-L1/CTLA-4双抗KN046联合阿昔替尼一线治疗晚期非小细胞肺癌(NSCLC)的Ⅱ期临床研究数据。
2024年第47届圣安东尼奥乳腺癌研讨会(SABCS)在美国圣安东尼奥举行。该会议上公布了维迪西妥单抗治疗HER2阳性存在肝转移的晚期乳腺癌患者Ⅲ期临床研究数据,这是全球首个证实HER2 ADC在HER2阳性存在肝转移的晚期乳腺癌患者中取得阳性结果的确证性Ⅲ期研究。该试验旨在评价维迪西妥单抗对比拉帕替尼联合卡培他滨治疗...
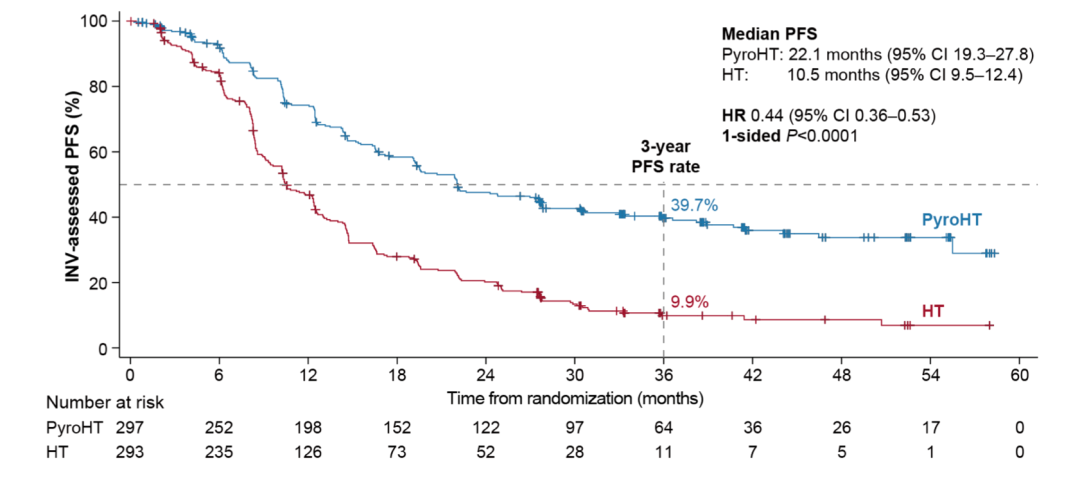
2024年第47届圣安东尼奥乳腺癌研讨会(SABCS)在美国圣安东尼奥举行。该会议上公布了中国医学科学院肿瘤医院徐兵河院士领衔的III期PHILA研究延长两年随访后的无进展生存期(PFS)最终分析。该试验旨在评估吡咯替尼+曲妥珠单抗+多西他赛方案对比安慰剂联合曲妥珠单抗和多西他赛一线治疗HER2阳性复发/转移性乳腺癌的...
肺癌是全球癌症相关死亡的主要原因,严重威胁着我国居民的生命健康。根据组织病理学特点不同,肺癌可分为非小细胞肺癌(NSCLC)和小细胞肺癌(SCLC),非小细胞肺癌(NSCLC)是最常见的肺癌类型,占所有肺癌病例的约85%。EGFR突变是非小细胞肺癌患者中常见的驱动基因突变,过去十年中,EGFR酪氨酸激酶抑制剂(TKI)...
2024年欧洲肿瘤内科学会亚洲年会(ESMO ASIA)上报告了JMT101联合奥西替尼治疗经典EGFR突变非小细胞肺癌(NSCLC)的Ⅱ期BOOSTER研究结果。
12月9日,第一三共宣布美国食品药品监督管理局(FDA)授予 Datopotamab deruxtecan (Dato-DXd)突破性疗法认定,用于治疗接受 EGFR 酪氨酸激酶抑制剂 (TKI) 和铂类化疗期间或之后出现疾病进展的局部晚期或转移性表皮生长因子受体突变 (EGFR 突变) 非小细胞肺癌 (NSCLC) ...
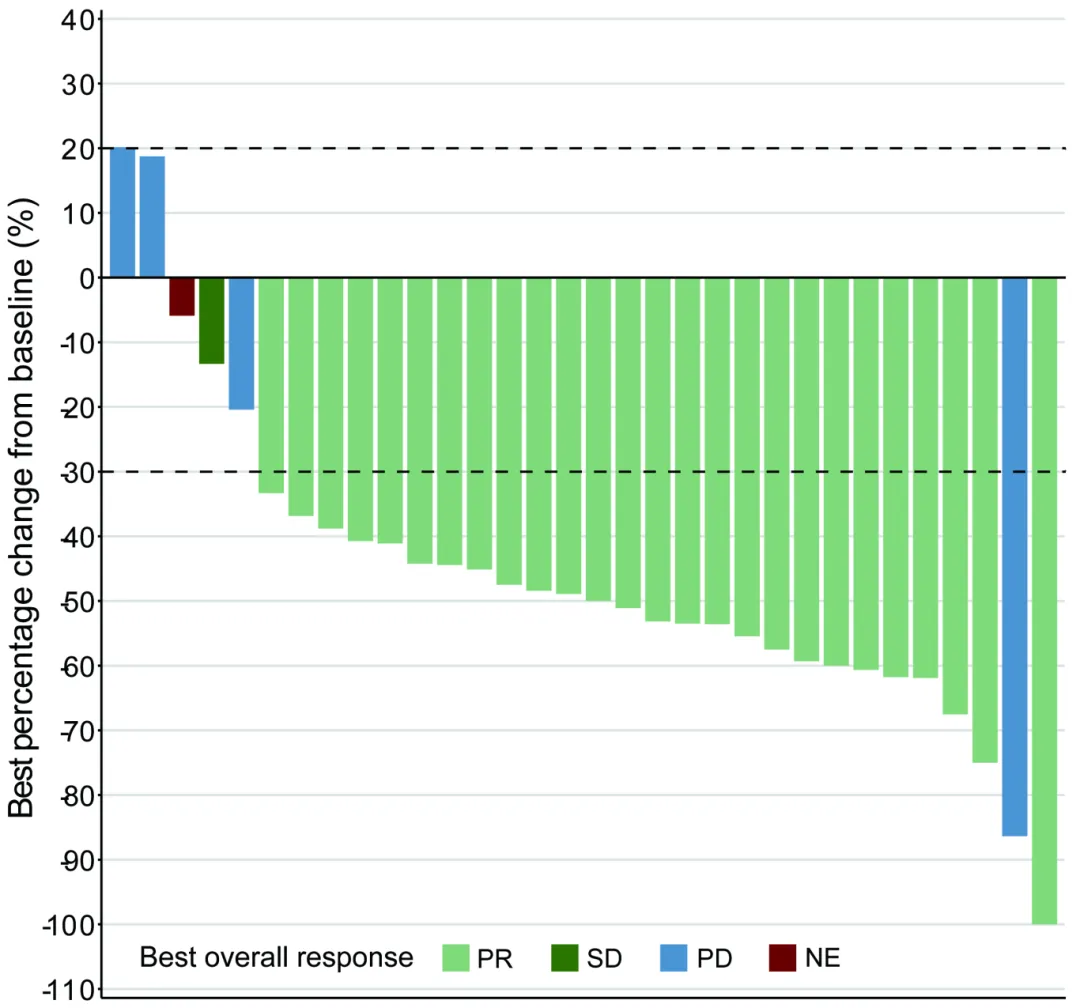
12月2日,欧洲肿瘤内科学会(ESMO)官方期刊《Lung Cancer》发表了新型肺癌靶向药舒沃哲®(通用名:舒沃替尼片)的一项Ⅰ/Ⅱ期临床研究的汇总分析最新数据。