热门推荐
- 精 日本上市佐妥昔单抗(Zolbetuximab),claudin (CLDN)18.2阳性胃癌患者迎来新药
- 精 疾病控制率高达90.9%!KRAS G12C抑制剂出击结直肠癌、非小细胞肺癌!
- 精 重磅!“治愈”肺癌更进一步!ALK抑制剂阿来替尼无病生存率高达93.8%!
- 精 85%患者的病情得到控制!KRAS G12C突变的患者有前景的治疗选择
- 精 HER2阳性实体瘤患者命运将改写!DS-8201再获FDA批准,不限癌种!
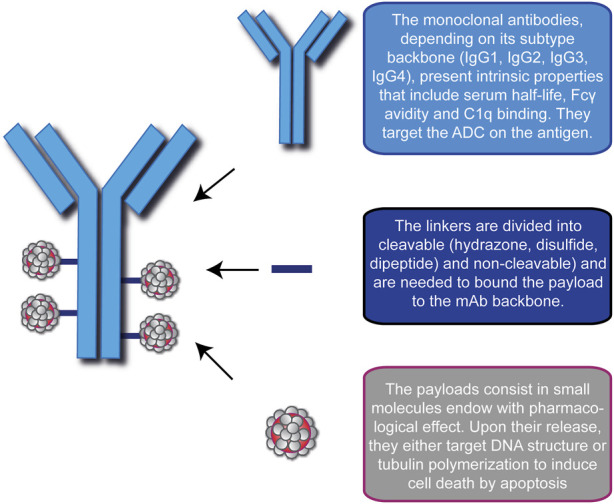
- 精 惊喜!无侵袭性癌生存率达到88.3%,一文读懂15款抗体偶联ADC药物
- 精 复发风险降低60%!特瑞普利单抗注射液再填适应症,我国首个、全球第二个获批的肺癌围手术期疗法
- 精 好消息!21款抗肿瘤药物纳入医保目录!但CAR-T产品无缘此次医保名单!
- 精 NTRK融合让众多实体瘤战栗,成为击败肿瘤的重磅武器
- 精 奥布替尼(Orelabrutinib)广受认可,让更多血液系统肿瘤患者获益
- 精 首款RET抑制剂普拉替尼给非小细胞肺癌患者带来希望
- 精 肿瘤和免疫的关系如何?CAR-T细胞疗法全球上市有9款
- 精 收藏 | 不能错过的胃癌的药物治疗大全!
- 精 KRAS基因靶点药物不间断研究中
- 精 仑伐替尼一种重要的靶向药
- 精 “不完美心动”——干细胞叫嚣“心衰”
- 精 伏美替尼 (Furmonertinib)第三代EGFR-TKI强势来袭
- 精 一文教会你BRCA突变和PAPR抑制剂的关系
- 精 国家药监局批准三款新药上市!!!攻克癌症不再天方夜谭!
- 精 中国首款自主研发的CAR-T细胞治疗伊基奥伦赛注射液获批上市
- 精 培美曲塞
资讯列表
2024年12月9日,2024年欧洲肿瘤内科学会亚洲年会(ESMO Asia)大会上报道了IBI343治疗晚期胰腺导管腺癌I期临床(NCT05458219)最新数据。
日本厚生劳动省已于2024年3月正式批准佐妥昔单抗日本上市,在欧盟批准之前,英国药品和保健品监管机构已于2024年8月批准。安斯泰来已向全球其他注册监管部门递交了上市申请,目前这些申请正在评审阶段。
12月3日,国家药品监督管理局(NMPA)批准呋喹替尼(爱优特)联合信迪利单抗注射液(达伯舒)用于治疗既往系统性抗肿瘤治疗后失败且不适合进行根治性手术治疗或根治性放疗的晚期错配修复完整 (pMMR) 的子宫内膜癌患者。
近日,2024年欧洲肿瘤内科学会亚洲年会(ESMO Asia)在新加坡召开。该会议上,复旦张江展示了抗Her2抗体偶联BB05药物(注射用FDA022抗体偶联剂)治疗晚期实体瘤患者的I期临床(NCT05564858)研究结果。
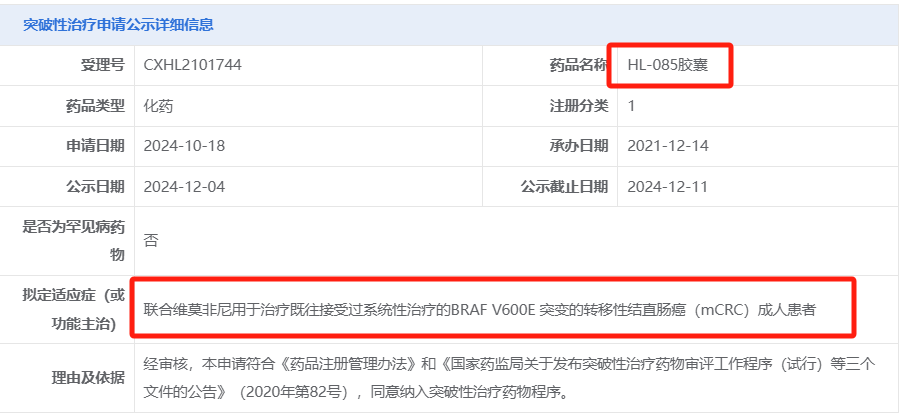
12月4日,国家药品监督管理局药品审评中心(CDE)显示:科州制药研发的HL-085胶囊拟纳入突破性治疗,拟定适应症为联合维莫非尼用于治疗既往接受过系统性治疗的BRAF V600E突变的转移性结直肠癌(mCRC)成人患者。
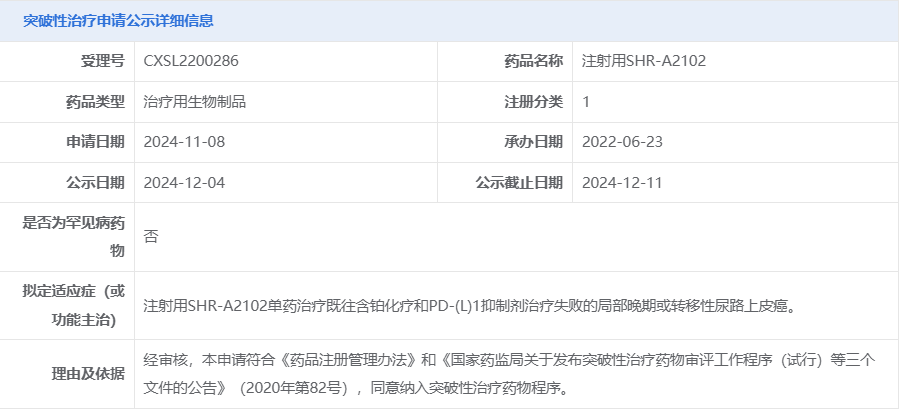
12月4日,国家药品监督管理局药品审评中心(CDE)显示:恒瑞医药SHR-A2102拟纳入突破性治疗品种,适应症为单药治疗既往含铂化疗和PD-(L)1抑制剂治疗失败的局部晚期或转移性尿路上皮癌。
12月06日,映恩生物在2024年欧洲肿瘤内科学会亚洲年会(ESMO Asia)上公布了DB-1311/BNT324(靶向B7H3的创新ADC分子)全球I/IIa期临床试验(NCT05914116,CTR20232835)的首批数据。
12月4日,美国食品药品监督管理局(FDA)批准度伐利尤单抗(durvalumab) 用于治疗接受铂类同步放化疗(cCRT)后病情未进展的局限期小细胞肺癌(LS-SCLC)成人患者。